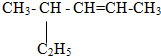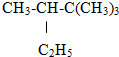题目内容
在标准状况下,18gCO和CO2的混合气体完全燃烧后得到11.2LCO2.则原混合气体的密度是 ;原混合气体中,CO的质量是 g,CO2的体积是 ,碳原子和氧原子的个数比为 .
考点:物质的量的相关计算
专题:计算题
分析:根据ρ=
计算混合气体的密度,令CO和CO2的物质的量分别为xmol、ymol,根据二者质量及体积列方程计算解答.
| m |
| V |
解答:
解:混合气体的密度=
=1.6g/L,
令CO和CO2的物质的量分别为xmol、ymol,根据二者质量及体积,则:
解得x=0.25 y=0.25
原混合气体中,CO的质量是0.25mol×28g/mol=7g,
标况下,CO2的体积是0.25mol×22.4L/mol=5.6L,
碳原子和氧原子的个数比为(0.25mol+0.25mol):(0.25mol+0.25mol×2)=2:3,
故答案为:1.6g/L;7;5.6L;2:3.
| 18g |
| 11.2L |
令CO和CO2的物质的量分别为xmol、ymol,根据二者质量及体积,则:
|
解得x=0.25 y=0.25
原混合气体中,CO的质量是0.25mol×28g/mol=7g,
标况下,CO2的体积是0.25mol×22.4L/mol=5.6L,
碳原子和氧原子的个数比为(0.25mol+0.25mol):(0.25mol+0.25mol×2)=2:3,
故答案为:1.6g/L;7;5.6L;2:3.
点评:本题考查混合物计算,侧重对物质的量有关计算考查,比较基础,注意对基础知识的理解掌握.

练习册系列答案
相关题目
下列各组物质之间通过一步就能实现如图所示转化的是( )
| 物质编号 | 物质转化关系 | a | b | c | d |
| ① | 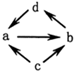 | Na2O | Na2O2 | Na | NaOH |
| ② | Al2O3 | NaAlO2 | Al | Al(OH)3 | |
| ③ | FeCl2 | FeCl3 | Fe | CuCl2 | |
| ④ | NO | NO2 | N2 | HNO3 |
| A、①② | B、②③. | C、②④ | D、①③ |
2011年12月5日,环保部制定的《环境空气质量标准》第二次公开征求意见结束,大家普遍赞成将PM2.5(PM2.5是指大气中直径接近于2.5×10-6m 的颗粒物)纳入常规空气质量评价.下列有关PM2.5的说法,不正确的是( )
| A、PM2.5表面积大,能吸附大量的有毒、有害物质 |
| B、PM2.5在空气中形成了气溶胶 |
| C、实施绿化工程,可以有效地防治PM2.5污染 |
| D、研制开发燃料电池汽车,降低机动车尾气污染,某种程度可以减少PM2.5污染 |
两种气态烷烃的混合物,在标准状况下其密度为1.03g?L-1,则关于该混合物组成的说法正确的是( )
| A、一定有甲烷 |
| B、一定有乙烷 |
| C、不可能是甲烷和乙烷的混合物 |
| D、可能是乙烷和丙烷的混合物 |