题目内容
(10分)榴石矿石可以看作由CaO、FeO、Fe2O3、Al2O3、SiO2组成。工业上对其进行综合利用的流程如下:
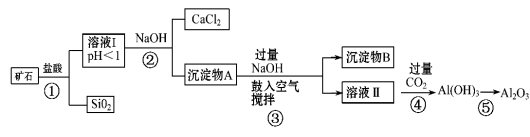
(1)SiO2的用途广泛,试写出其中的一种重要用途 ;
(2)溶液Ⅰ中除了Ca2+外,还含有的金属阳离子有 ;
(3)步骤③中NaOH参加反应的离子方程式是 ,
鼓入空气并充分搅拌的目的是(用化学方程式表示): 。
(4)在工业生产中,步骤④通入过量CO2而不加入盐酸的原因是 ________。
(10分) (1) 制造光导纤维 (2) Al3+、Fe3+、Fe2+
(3)Al(OH)3+OH- [Al(OH)4]- 4Fe(OH)2 + O2 + 4H2O == 4Fe(OH)3
[Al(OH)4]- 4Fe(OH)2 + O2 + 4H2O == 4Fe(OH)3
(4)使用CO2可以避免盐酸过量导致生成的Al(OH)3溶解,同时CO2容易制取,价格便宜
【解析】
试题分析:(1)二氧化硅的用途很广泛,可用作制光导纤维、是生产玻璃的原料等;
(2)CaO、FeO、Fe2O3、Al2O3、SiO2中与盐酸不发生反应的是二氧化硅,其余均与盐酸反应生成盐和水,所以溶液I中除了Ca2+外,还含有的金属阳离子有Al3+、Fe3+、Fe2+;
(3)沉淀物为氢氧化亚铁、氢氧化铁、氢氧化铝,加入过量的氢氧化钠溶液,则氢氧化铝沉淀溶解,发生的离子方程式为Al(OH)3+OH- [Al(OH)4]-;鼓入空气并充分搅拌的目的是使氢氧化亚铁全部转化为氢氧化铁沉淀,离子方程式为4Fe(OH)2 + O2 + 4H2O == 4Fe(OH)3;
[Al(OH)4]-;鼓入空气并充分搅拌的目的是使氢氧化亚铁全部转化为氢氧化铁沉淀,离子方程式为4Fe(OH)2 + O2 + 4H2O == 4Fe(OH)3;
(4)因为溶液II中存在偏铝酸根离子,偏铝酸根离子与二氧化碳反应生成氢氧化铝,不溶于碳酸,而溶于盐酸,所以通入二氧化碳气体可使Al元素全部转化为氢氧化铝沉淀,同时二氧化碳容易制取u,价格便宜。
考点:考查对流程图的分析,Al的化合物性质的应用



 O2(g)
O2(g) NO(g)+
NO(g)+ H2O(g); ΔH=-a kJ·mol-1
H2O(g); ΔH=-a kJ·mol-1 O2(g)
O2(g) 2NH3(g);△H<0,为使氨的产率提高,理论上应采取低温高压的措施
2NH3(g);△H<0,为使氨的产率提高,理论上应采取低温高压的措施