题目内容
碘盐的主要成分是KIO3和NaCl,KIO3在工业上可用电解法制取,以石墨和铁为电极,电解KI溶液,反应方程式为KI+3H2O=KIO3 +3H2↑。下列有关说法中正确的是
- A.电解时,石墨作阴极,铁作阳极
- B.电解时,在阴极上产生KIO3
- C.电解后电解质溶液pH变大
- D.电解中每转移0.6mol e-,理论上可得到0.1mol无水KIO3晶体
D
试题分析:A、铁作阳极,则铁放电Fe-2e-=Fe2-,I-无法转变为IO3-,错误; B、I-转变为IO3-,I由-1价升高到+5价,失去e-(氧化反应)在阳极上发生,错误;C、反应方程式为KI+3H2O=KIO3 +3H2↑,无酸碱的消耗和生成,溶液pH不变,错误; D、根据题中反应,每转移6mol e-,理论上可得到1mol KIO3,若转移0.6mol e-,理论上可得到0.1mol无水KIO3,正确。
考点:考查电解池与氧化还原反应相关知识。
试题分析:A、铁作阳极,则铁放电Fe-2e-=Fe2-,I-无法转变为IO3-,错误; B、I-转变为IO3-,I由-1价升高到+5价,失去e-(氧化反应)在阳极上发生,错误;C、反应方程式为KI+3H2O=KIO3 +3H2↑,无酸碱的消耗和生成,溶液pH不变,错误; D、根据题中反应,每转移6mol e-,理论上可得到1mol KIO3,若转移0.6mol e-,理论上可得到0.1mol无水KIO3,正确。
考点:考查电解池与氧化还原反应相关知识。

练习册系列答案
 七星图书口算速算天天练系列答案
七星图书口算速算天天练系列答案
相关题目
2011年3月18日至19日,受“吃碘盐能防止核辐射”等谣言的影响,我国部分地区出现抢购食盐现象。已知碘盐的主要成分是KIO3和NaCl,KIO3与NaHSO3发生反应:2KIO3 + 6NaHSO3 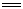 2KI + 3Na2SO4 + 3H2SO4,下列说法中不正确的是( )
2KI + 3Na2SO4 + 3H2SO4,下列说法中不正确的是( )
| A.23Na37Cl中质子数和中子数之比是7:8 | B.KIO3和NaHSO3都是强电解质 |
| C.KIO3作氧化剂发生氧化反应 | D.生成1mo1 KI时,转移6 mo1电子 |
 2KI
+ 3Na2SO4 + 3H2SO4,下列说法中不正确的是( )
2KI
+ 3Na2SO4 + 3H2SO4,下列说法中不正确的是( )