题目内容
(11分)某学生欲用已知物质的量浓度的盐酸来测定未知物质的量浓度的氢氧化钠溶液,请填写下列空白:(1)选用的指示剂是 。
(2)用标准的盐酸溶液滴定待测的氢氧化钠溶液时,左手把握酸式滴定管的活塞,右手摇动锥形瓶,眼睛注视______________________。
(3)下列操作中可能使所测氢氧化钠溶液的浓度数值偏低的是_______________。
| A.酸式滴定管未用标准盐酸溶液润洗就直接注入标准盐酸溶液 |
| B.滴定前盛放氢氧化钠溶液的锥形瓶用蒸馏水洗净后没有干燥 |
| C.酸式滴定管在滴定前有气泡,滴定后气泡消失 |
| D.读取盐酸体积时,开始仰视读数,滴定结束时俯视读数 |
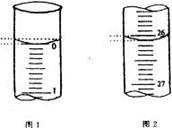
请将数据填入下面表格的空白处。
| 滴定次数 | 待测氢氧化钠溶液的体积/ mL | 0.1000 mol/L 盐酸的体积/ mL | ||
| 滴定前刻度 | 滴定后刻度 | 溶液体积/ mL | ||
| 第一次 | 25.00 | | | |
| 第二次 | 25.00 | 2.00 | 28.08 | 26.08 |
| 第三次 | 25.00 | 0.22 | 26.34 | 26.12 |
(6)滴定终点的判定依据是 。
25、(1)甲基橙 (2)眼睛应注意锥形瓶内颜色的变化(3)D
(4)0.00 、26.10 、26.10 (5)0.104 4 mol/L (6)溶液从黄色变为橙色,半分钟内不变色。
解析试题分析:(1)甲基橙是酸碱指示剂,pH值变色范围3.1(红)-4.4(黄),选甲基橙
(2)眼睛观察的是锥形瓶内指示剂颜色的变化,而不是滴定管中液体的体积变化;判断滴定终点时,注意在指示剂颜色发生变化后,半分钟内不再复原,停止滴定,答案为眼睛应注意锥形瓶内颜色的变化;
(3)A.由于未用标准液润洗,导致消耗盐酸的体积比实际上要大,测定的氢氧化钠溶液的浓度偏高。B.无影响;C. 酸式滴定管在滴定前有气泡,滴定后气泡消失,直接导致读数比实际值偏大,使测定的氢氧化钠溶液的浓度偏高;D. 读取盐酸体积时,开始仰视读数,滴定结束时俯视读数,导致读数比实际上偏小,使测定的氢氧化钠溶液的浓度偏低;选D。
(4)由图可知:滴定前刻度0.00,滴定后刻度26.10,溶液体积26.10;
(5)取这三次盐酸体积的平均值:V=(26.10+26.08+26.12)/3= 26.10(mL),其浓度为0.100 0 mol/L,待测氢氧化钠溶液的体积为25.00 mL,则该氢氧化钠溶液的物质的量浓度c(NaOH)=c(盐酸)×V(盐酸) /V(NaOH)=0.104 4 mol/L;
(6)滴定终点的判定依据是溶液从黄色变为橙色,半分钟内不变色。
考点:考查酸碱中和滴定。

 学而优衔接教材南京大学出版社系列答案
学而优衔接教材南京大学出版社系列答案下列化学用语表示正确的是
A.S2-的离子结构示意图: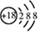 |
| B.次氯酸的结构式:H—O—CI |
C.水分子的比例模型: |
D.NCI3的电子式: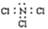 |
现有常温时pH=1的某强酸溶液10 mL,下列操作能使溶液的pH变成2的是
| A.加水稀释成100 mL。 |
| B.加入10 mL的水进行稀释。 |
| C.加入10 mL 0.01 mol/L的NaOH溶液。 |
| D.加入10 mL 0.01 mol/L的HCl溶液。 |
(10分)用0.2000mol/L NaOH溶液滴定未知浓度的盐酸,其操作可分解为如下几步:
(A)移取15.00mL待测的盐酸溶液注入洁净的锥形瓶,并加入2-3滴酚酞
(B)用标准NaOH溶液润洗碱式滴定管2-3次
(C)把盛有标准溶液的滴定管固定好,使滴定管尖嘴充满溶液
(D)取标准溶液注入滴定管至0刻度以上2-3cm
(E)调节液面至0或0刻度以下,记下读数
(F)把锥形瓶放在滴定管下面,用标准NaOH溶液滴定至终点,记下滴定管液面的刻度
完成以下各空:
(1)正确操作的顺序是B→_____→_____→_____→A→F;
(2)三次滴定消耗NaOH溶液的体积如下:
| 实验序号 | 1 | 2 | 3 |
| 消耗NaOH溶液的体积(mL) | 20.05 | 20.00 | 19.95 |
(3)用标准的NaOH溶液滴定未知浓度的盐酸,下列情况可能造成测定结果偏高的是: 。
A.配制标准溶液时称量的氢氧化钠固体中混有Na2CO3杂质
B.滴定终点读数时,俯视滴定管的刻度,其它操作均正确
C.盛装待测液的锥形瓶用蒸馏水洗过,未用待测液润洗
D.滴定到终点读数时发现滴定管尖嘴处悬挂一滴溶液
9分)某学生用已知物质的量浓度的盐酸来测定未知浓度的氢氧化钠溶液时,选择甲基橙作指示剂。
请填写下列空白:
(1)酸式滴定管用蒸馏水洗净后,接下来应该进行的操作是_________。
(2)用标准盐酸溶液滴定时,应将标准盐酸溶液注入________(填“甲”或“乙”)中。
(3)用标准的盐酸滴定待测的氢氧化钠溶液时,左手握酸式滴定管的活塞,右手轻轻摇动锥形瓶,眼睛注视_______________________________________________________。
(4)直到因加入一滴盐酸后,溶液颜色由________色变为________色,并在30 s内不变,即为终点。
(5)下列操作中可能使所测氢氧化钠溶液浓度偏大的是________。
| A.酸式滴定管未用标准盐酸润洗,直接装入标准盐酸。 |
| B.酸式滴定管滴定前有气泡,滴定后气泡消失。 |
| C.滴定前盛放氢氧化钠溶液的锥形瓶用蒸馏水洗净后未干燥。 |
| D.读取盐酸体积开始时仰视读数,滴定结束后俯视读数。 |
化学家认为石油、煤作为能源使用时,燃烧了“未来的原始材料”。下列对上述观点理解正确的是
| A.大力提倡使用廉价化石燃料作为能源 |
| B.化石燃料属于可再生能源,不影响可持续发展 |
| C.应更多地利用石油和煤生产基本化工原料 |
| D.研发新型催化剂,提高石油和煤中各组分的燃烧热 |
聚丙烯酸酯类涂料是目前市场上流行的墙面涂料之一,它具有弹性好、不易老化、耐擦洗、色泽亮丽等优点.下边是聚丙烯酸酯的结构简式,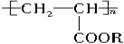
它属于
①无机化合物 ②有机化合物 ③高分子化合物 ④离子化合物 ⑤共价化合物
| A.①③④ | B.①③⑤ | C.②③⑤ | D.②③④ |
下列各种玻璃仪器中,不能进行加热的是
| A.蒸馏烧瓶 | B.烧杯 | C.蒸发皿 | D.容量瓶 |