题目内容
10.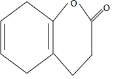 的同分构体中只有一个支链且能与NaHCO3溶液反应的芳香族化合物有(不考虑立体异构)( )
的同分构体中只有一个支链且能与NaHCO3溶液反应的芳香族化合物有(不考虑立体异构)( )| A. | 1种 | B. | 2种 | C. | 3种 | D. | 4种 |
分析  分子式为C9H10O2,其不饱和度为$\frac{9×2+2-10}{2}$=5;能与NaHCO3溶液反应,说明该有机物分子中含有官能团-COOH,芳香族化合物中一定含有苯环,苯环中含有6个C,不饱和度为4,羧基的不饱和度为1,说明其它结构中不含不饱和键,只有一个支链的为:-CH2CH2COOH或-CH(CH3)COOH,据此进行判断其可能结构.
分子式为C9H10O2,其不饱和度为$\frac{9×2+2-10}{2}$=5;能与NaHCO3溶液反应,说明该有机物分子中含有官能团-COOH,芳香族化合物中一定含有苯环,苯环中含有6个C,不饱和度为4,羧基的不饱和度为1,说明其它结构中不含不饱和键,只有一个支链的为:-CH2CH2COOH或-CH(CH3)COOH,据此进行判断其可能结构.
解答 解: 分子式为C9H10O2,其不饱和度为$\frac{9×2+2-10}{2}$=5;能与NaHCO3溶液反应,说明该有机物分子中含有官能团-COOH,芳香族化合物中一定含有苯环,苯环中含有6个C,不饱和度为4,羧基的不饱和度为1,说明其它结构中不含不饱和键,只有一个支链的为:-CH2CH2COOH或-CH(CH3)COOH,所以符合条件的芳香族化合物有2种,故选B.
分子式为C9H10O2,其不饱和度为$\frac{9×2+2-10}{2}$=5;能与NaHCO3溶液反应,说明该有机物分子中含有官能团-COOH,芳香族化合物中一定含有苯环,苯环中含有6个C,不饱和度为4,羧基的不饱和度为1,说明其它结构中不含不饱和键,只有一个支链的为:-CH2CH2COOH或-CH(CH3)COOH,所以符合条件的芳香族化合物有2种,故选B.
点评 本题考查同分异构体数目的求算,题目难度中等,明确官能团以及取代基的分类是解答本题的关键.

练习册系列答案
相关题目
20.下列各组离子或分子在指定环境中一定能大量共存的是( )
| A. | 使石蕊变红的溶液中:Ag(NH3)2+、Fe3+、Cl-、NO3- | |
| B. | 常温下c(H+)=10-14mol/L的溶液中:Na+、AlO2-、SO32-、S2- | |
| C. | “84”消毒液中:NO3-、Cl-、Ca2+、H+ | |
| D. | 常温时,在中性溶液中:Na+、Fe3+、NO3-、Cl- |
1.某醇C5H11OH是由烯烃C5H10与水发生加成反应制得的,则此醇的结构可能有( )
| A. | 5种 | B. | 6种 | C. | 7种 | D. | 8种 |
18.短周期主族元素X、Y、Z、W的原子序数依次增大.X与W同主族,X、W的单质在标准状况下的状态不同.Y是空气中含量最高的元素,Z原子最外层电子数是其内层电子总数的3倍,Z2-与W+有相同的电子层结构.下列说法正确的是( )
| A. | 原子半径大小:r(W)>r(Z)>r(Y)>r(X) | |
| B. | 元素Y的简单气态氢化物的热稳定性和熔沸点都比Z的高 | |
| C. | 化合物X2Z2与 W2Z2所含化学键类型完全相同 | |
| D. | 只含X、Y、Z三种元素组成物质的水溶液可能呈酸性或碱性 |
15.生活中不少人爱追求“档次“,其中实现的关键是物质,下列叙述正确的是( )
| A. | “百年陈酒“说明储存的时间长,陈酒中是不掺杂一滴水的 | |
| B. | “千年寿龟”身上的外壳主要成分是纤维素 | |
| C. | “如意蔬菜”是一种用陶瓷制作的装饰物,其主要成分属于硅酸盐产品 | |
| D. | “黄金大米”颜色金黄,富含锌、铁、钙等微量元素 |
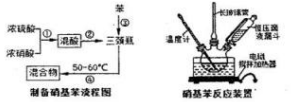
2.硝基苯是医药和染料的中间体,还是有机溶剂.反应流程、装置如下.
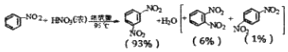
制备硝基苯时还可能发生下列副反应:
有关数据如下表
(1)制备硝基苯的反应式C6H6+HNO3$→_{50-60℃}^{浓硫酸}$C6H5NO2+H2O;
(2)步骤①配置混酸:取100 mL烧杯,用20mL浓硫酸与18mL浓硝酸配置混合酸,操作是:在烧杯中先加入18mL浓硝酸,再沿烧杯壁注入20mL浓硫酸,并不断搅拌、冷却;把配好的混合酸加入恒压漏斗中;最后在三颈烧瓶中加入18mL苯.
(3)在室温下向三颈瓶中的苯中逐滴加入混酸,边滴边搅拌,混合均匀、加热.上图中的加热方式称为水浴加热;反应温度控制在50~60℃的原因是减少(或防止)副反应发生或减少硝酸分解.
硝基苯的提纯步骤为:

(4)步骤⑤表明混合物中有苯和硝基苯的操作和现象是混合物倒入蒸馏水中,液体分为三层.
(5)验证步骤⑥中液体已洗净的操作和现象是:取最后一次洗涤液,向溶液中加入氯化钙溶液,有白色沉淀生成,说明洗涤干净;为了得到更纯净的硝基苯,还须向液体中加入无水CaCl2除去水,然后蒸馏(填操作名称).
(6)设计实验证明“粗产品2”中含二硝基苯测定粗产品的密度大于1.205g•cm-3.
(7)用铁粉、稀盐酸与硝基苯(用Ph-NO2表示)反应可生成染料中间体苯胺(Ph-NH2),其反应的化学方程式为Ph-NO2+3Fe+6HCl→Ph-NH2+3FeCl2+2H2O.

制备硝基苯时还可能发生下列副反应:

有关数据如下表
| 物质 | 熔点/℃ | 沸点/℃ | 密度(20℃)/g•cm-3 | 水溶性 |
| 苯 | 5.5 | 80 | 0.88 | 微溶 |
| 硝基苯 | 5.7 | 210.9 | 1.205 | 难溶 |
| 1,3-二硝基苯 | 89 | 301 | 1.57 | 微溶 |
(2)步骤①配置混酸:取100 mL烧杯,用20mL浓硫酸与18mL浓硝酸配置混合酸,操作是:在烧杯中先加入18mL浓硝酸,再沿烧杯壁注入20mL浓硫酸,并不断搅拌、冷却;把配好的混合酸加入恒压漏斗中;最后在三颈烧瓶中加入18mL苯.
(3)在室温下向三颈瓶中的苯中逐滴加入混酸,边滴边搅拌,混合均匀、加热.上图中的加热方式称为水浴加热;反应温度控制在50~60℃的原因是减少(或防止)副反应发生或减少硝酸分解.
硝基苯的提纯步骤为:

(4)步骤⑤表明混合物中有苯和硝基苯的操作和现象是混合物倒入蒸馏水中,液体分为三层.
(5)验证步骤⑥中液体已洗净的操作和现象是:取最后一次洗涤液,向溶液中加入氯化钙溶液,有白色沉淀生成,说明洗涤干净;为了得到更纯净的硝基苯,还须向液体中加入无水CaCl2除去水,然后蒸馏(填操作名称).
(6)设计实验证明“粗产品2”中含二硝基苯测定粗产品的密度大于1.205g•cm-3.
(7)用铁粉、稀盐酸与硝基苯(用Ph-NO2表示)反应可生成染料中间体苯胺(Ph-NH2),其反应的化学方程式为Ph-NO2+3Fe+6HCl→Ph-NH2+3FeCl2+2H2O.
19.下列有关溶液组成的描述合理的是( )
| A. | 澄清透明溶液中可能大量存在:Cu2+、Mg2+、NO3-、SO42- | |
| B. | 加入KSCN显红色的溶液中可能大量存在:K+、NH4+、Cl-、I- | |
| C. | 加入A1能放出大人量H2的溶液中可能大量存在:NH4+、Fe2+、NO3-、SO42- | |
| D. | 常温下,$\frac{c(O{H}^{-})}{c({H}^{+})}$=1×l0-12的溶液中可能大量存在:K+、AlO2-、CO32-、Na+ |