题目内容
10.下列说法正确的是( )| A. | 测定HCl和NaOH中和反应的反应热时,单次实验均应测量3个温度,即盐酸起始温度、NaOH溶液起始温度和反应终止温度 | |
| B. | 若2C(s)+O2(g)=2CO(g)△H=-221.0kJ/mol,则碳的燃烧热为110.5KJ/mol | |
| C. | 需要加热的反应一定是吸热反应,常温下能发生的反应一定是放热反应 | |
| D. | 已知I:反应H2(g)+Cl2(g)=2HCl(g);△H=-akJ/mol II:  且a、b、c均大于零,则断开1molH-Cl键所需的能量为2(a+b+c)kJ/mol |
分析 A.测定中和热的方法是利用量热计测定开始和反应终止时的温度计算得到;
B.C的燃烧热中生成稳定氧化物应该为二氧化碳;
C.放热反应有的也需要一定条件才能发生;
D.依据反应焓变△H=反应物键能总和-生成物键能总和计算分析.
解答 解:A.中和热测定实验中,依据Q=-c(T2-T1)计算反应热,需要测定反应前酸碱溶液温度或反应后最高温度,总共3个温度,故A正确;
B.C对应的稳定氧化物为二氧化碳,该反应生成CO,该反应热不是C的燃烧热,故B错误;
C.放热反应有的也需要一定条件才能发生,如氢气和氧气需要点燃发生反应,故C错误;
D.依据反应焓变△H=反应物键能总和-生成物键能总和计算分析,△H=b+c-2x=-akJ/mol,x=$\frac{a+b+c}{2}$mol/L,则断开1molH-Cl键所需吸收能量为$\frac{a+b+c}{2}$kJ,故D错误;
故选A.
点评 本题考查反应热与焓变的综合应用,题目难度中等,明确燃烧热的概念为解答关键,注意掌握化学反应与能量变化的关系,试题有利于提高学生的灵活应用能力.

练习册系列答案
相关题目
20. 已知某可逆反应:mA(g)+nB(g)?pC(g)△H=Q kJ•mol-1,在密闭容器中进行,如图表示在不同时间t、温度T、压强P与反应物B的百分含量的关系曲线,下列判断正确的是( )
已知某可逆反应:mA(g)+nB(g)?pC(g)△H=Q kJ•mol-1,在密闭容器中进行,如图表示在不同时间t、温度T、压强P与反应物B的百分含量的关系曲线,下列判断正确的是( )
 已知某可逆反应:mA(g)+nB(g)?pC(g)△H=Q kJ•mol-1,在密闭容器中进行,如图表示在不同时间t、温度T、压强P与反应物B的百分含量的关系曲线,下列判断正确的是( )
已知某可逆反应:mA(g)+nB(g)?pC(g)△H=Q kJ•mol-1,在密闭容器中进行,如图表示在不同时间t、温度T、压强P与反应物B的百分含量的关系曲线,下列判断正确的是( )| A. | T1<T2,P1>P2,m+n>p△Η<0 | B. | T1>T2,P1<P2,m+n<p△Η>0 | ||
| C. | T1<T2,P1>P2,m+n<p△Η<0 | D. | T1>T2,P1<P2,m+n>p△Η>0 |
5.下列有机坊与其名称相符的是( )
| A. |  :2-甲基丙烯 :2-甲基丙烯 | B. | (CH3)2CHCH(CH3)2:1,4-而甲基丁烷 | ||
| C. | 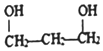 :1,3-二丙醇 :1,3-二丙醇 | D. | 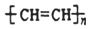 :聚乙烯 :聚乙烯 |
15.X、Y、Z、R、W是原子序数依次增大的五种短周期元素.Y和R同主族,可组成共价化合物RY2,Y和Z最外层电子数之和与W的最外层电子数相同.250C时,0.1mol/L X和W形成的化合物的水溶液pH=1.下列说法中正确的是( )
| A. | Y、Z、W三种元素组成的化合物的水溶性一定显碱性 | |
| B. | 原子半径:X<Y<Z<R<W | |
| C. | R元素的最高价氧化物的水化物酸性最强 | |
| D. | Y和其他四种元素均可形成至少两种化合物(两种元素组成) |
2.某烃的结构简式为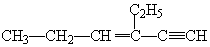 ,分子中含有四面体结构的碳原子数为a,在同一直线上的碳原子数为b,在同一平面内的碳原子数最多为c,则a、b、c分别为( )
,分子中含有四面体结构的碳原子数为a,在同一直线上的碳原子数为b,在同一平面内的碳原子数最多为c,则a、b、c分别为( )
 ,分子中含有四面体结构的碳原子数为a,在同一直线上的碳原子数为b,在同一平面内的碳原子数最多为c,则a、b、c分别为( )
,分子中含有四面体结构的碳原子数为a,在同一直线上的碳原子数为b,在同一平面内的碳原子数最多为c,则a、b、c分别为( )| A. | 4、3、6 | B. | 4、3、8 | C. | 2、5、4 | D. | 4、4、6 |
19.苹果酸的结构简式为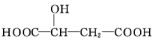 ,下列说法正确的是( )
,下列说法正确的是( )
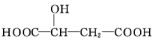 ,下列说法正确的是( )
,下列说法正确的是( )| A. | 苹果酸不能发生聚合反应 | |
| B. | 1 mol苹果酸与足量金属Na反应生成1 mol H2 | |
| C. | 苹果酸分子的核磁共振氢谱有四组峰,峰面积之比为1:1:2:2 | |
| D. | 苹果酸中能发生酯化反应的官能团有2种 |
20.短周期主族元素X、Y、Z、W的原子序数依次增大,X是地壳中含量最多的元素;Z原子的最外层电子数是其最内层电子数的$\frac{1}{2}$;W的最高正价和最低负价的代数和为0,下列说法正确的是( )
| A. | 原子半径:X<Y<Z<W | |
| B. | Z的氢化物中只含离子键 | |
| C. | 最高价氧化物对应水化物的酸性:Y<W | |
| D. | X和W两种元素形成的化合物,既能与强酸反应又能与强碱反应 |

 .
.