题目内容
10.已知如下物质的溶度积常数:FeS:Ksp=6.3×10-18;CuS:Ksp=1.3×10-36;ZnS:Ksp=1.6×10-24.下列说法正确的是( )| A. | 同温度下,CuS的溶解度大于ZnS的溶解度 | |
| B. | 将足量CuSO4溶解在0.1 mol•L-1的H2S溶液中,Cu2+能达到的最大浓度为1.3×10-35 mol•L-1 | |
| C. | 因为H2SO4是强酸,故CuSO4+H2S═CuS↓+H2SO4不能发生 | |
| D. | 除去工业废水中的Cu2+,可以选用FeS作沉淀剂 |
分析 三种物质的化学式形式相同,可以直接通过溶度积常数比较二者的溶解度,根据溶度积常数计算溶液中的离子浓度,从溶解平衡移动的角度分析.
解答 解:A.ZnS与CuS的化学式形式相同,可以直接通过溶度积常数比较二者的溶解度,Ksp越小,溶解度越小,故A错误;
B.将足量CuSO4溶解在0.1 mol•L-1的H2S溶液中,生成CuS沉淀后,溶液为硫酸铜溶液,Cu2+的最大浓度应为饱和溶液的浓度,故B错误;
C.由于CuS是难溶于酸的沉淀,反应符合复分解条件,能发生,故C错误;
D.FeS的溶度积大于CuS的溶度积,其溶解平衡的S2-浓度远大于CuS的S2-离子浓度,故加入FeS可以沉淀废水中的Cu2+,故D正确.
故选D.
点评 本题综合考查难溶电解质的溶解平衡问题,题目难度中等,注意把握溶度积的定义的理解和计算的应用,易错点为B.

练习册系列答案
相关题目
11.W是由短周期元素X、Y、Z组成的盐.X、Y、Z原子的最外层电子数依次增大,Z原子最外层电子数是内层电子数的3倍;X、Y原子最外层电子数之和等于Z原子的最外层电子数;Y、Z同周期且相邻,但与X不同周期.下列说法一定正确的是( )
| A. | 三种元素的最高正化合价中,Z的最大 | |
| B. | W溶液显碱性或中性 | |
| C. | 原子半径:X>Y>Z | |
| D. | Y的最高价氧化物对应的水化物是强酸. |
1. 25℃,电离平衡常数:
25℃,电离平衡常数:
回答下列问题:
(1)物质的量浓度为0.1mol/L的下列四种物质:a.Na2CO3,b.NaClO,c.CH3COONa,d.NaHCO3;pH由大到小的顺序是abdc(填编号)
(2)在Na2CO3溶液中通入少量的SO2气体,写出离子方程式2CO32-+SO2+H2O═2HCO3-+SO32-
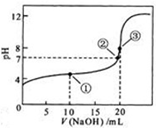
(3)用0.1000mol/L NaOH溶液滴定0.1000mol/L 20mL CH3COOH溶液,得到如图曲线在②时,溶液中离子浓度大小顺序为c(Na+)=c(CH3COO-)>c(H+)=c(OH-)
在①时,测得pH约为5,c(CH3COO-)-c(Na+)=10-5-10-9mol/L(填精确数值)
(4)常温下,CH3COOH与NH3.H2O的电离平衡常数均为1.8×10-5,则NH4HCO3溶液呈碱性.
溴水.
 25℃,电离平衡常数:
25℃,电离平衡常数:| 化学式 | CH3COOH | H2CO3 | HClO | H2SO3 |
| 电离平衡常数 | 1.8×10-5 | K1=4.3×10-7 K2=5.6×10-11 | 3.0×10-8 | K1=1.5×10-2 K2=1.0×10-7 |
(1)物质的量浓度为0.1mol/L的下列四种物质:a.Na2CO3,b.NaClO,c.CH3COONa,d.NaHCO3;pH由大到小的顺序是abdc(填编号)
(2)在Na2CO3溶液中通入少量的SO2气体,写出离子方程式2CO32-+SO2+H2O═2HCO3-+SO32-
(3)用0.1000mol/L NaOH溶液滴定0.1000mol/L 20mL CH3COOH溶液,得到如图曲线在②时,溶液中离子浓度大小顺序为c(Na+)=c(CH3COO-)>c(H+)=c(OH-)
在①时,测得pH约为5,c(CH3COO-)-c(Na+)=10-5-10-9mol/L(填精确数值)
(4)常温下,CH3COOH与NH3.H2O的电离平衡常数均为1.8×10-5,则NH4HCO3溶液呈碱性.
溴水.
18.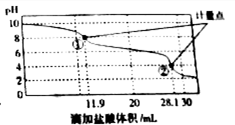 称取Na2CO3和NaHCO3混合物样品1.6226g,溶于水配成250.00ml溶液,取出该溶液25.00ml用 0.1mol•L-1 盐酸滴定,得到如图曲线.以下说法错误的是( )
称取Na2CO3和NaHCO3混合物样品1.6226g,溶于水配成250.00ml溶液,取出该溶液25.00ml用 0.1mol•L-1 盐酸滴定,得到如图曲线.以下说法错误的是( )
 称取Na2CO3和NaHCO3混合物样品1.6226g,溶于水配成250.00ml溶液,取出该溶液25.00ml用 0.1mol•L-1 盐酸滴定,得到如图曲线.以下说法错误的是( )
称取Na2CO3和NaHCO3混合物样品1.6226g,溶于水配成250.00ml溶液,取出该溶液25.00ml用 0.1mol•L-1 盐酸滴定,得到如图曲线.以下说法错误的是( )| A. | 样品中Na2CO3含量越高,起始pH也越大 | |
| B. | 计量点①中有关离子浓度关系为:c(HCO3-)>C(Cl-)>c(CO32-) | |
| C. | 计量点②溶液中有关离子浓度关系为:2(CO32-)+c(HCO3-)=C(H+)-c(OH-) | |
| D. | 此样品n(NaHCO3)=(28.1-11.9)×10-3mol |
15.目前污水处理厂用新型高效絮凝剂碱式硫酸铁[Fe(OH)SO4]来处理水中的悬浮颗粒物,采用微生物燃料电池使水中的有机物变成二氧化碳,从而使污水得到净化.
I.工业上利用废铁屑(含少量氧化铝、氧化铁等)生产碱式硫酸铁的工艺流程如图1:
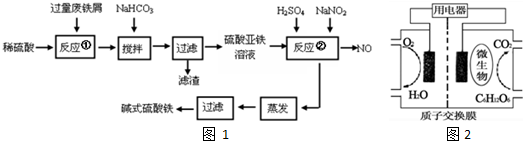
已知:25℃时部分阳离子以氢氧化物形式沉淀时溶液的pH见表:
回答下列问题:
(1)加入少量NaHCO3的目的是调节pH在4.4-7.5范围内,使溶液中Al 3+沉淀.
(2)若沉淀完全时溶液中金属离子浓度为1.0×10-5mol/L,则Ksp[Fe(OH)2]=1.0×10-15.
(3)在实际生产中,反应②常同时通入O2以减少NaNO2的用量,若标况下有33.6L O2参与反应,则相当于节约NaNO2的物质的量为6mol.
(4)该生产碱式硫酸铁的工艺过程中存在的明显缺点是会产生一氧化氮,会造成大气污染.
II.微生物燃料电池是以微生物作催化剂,以有机污水为燃料,将有机污水中的化学能直接转化为电能的一种装置.
(5)重庆大学研究出一种微生物燃料电池,可以将污水中的CH3COO-处理掉,
其总反应为:2CH3COOK+4H2O+8K2S2O8═4CO2↑+7H2SO4+9K2SO4,写出该微生物
燃料电池负极的电极反应式CH3COO-+2H2O-8e-=2CO2↑+7H+.
(6)以葡萄糖为燃料的微生物燃料电池结构示意图如图2:
①关于该电池的叙述,正确的有BD
A.电池的正极反应为:O2+2H2O+4e-═4OH-
B.在电池反应中,每消耗90克葡萄糖,经外电路通过的电子数为12NA
C.该电池能够在高温下工作
D.放电过程中,H+从负极区向正极区迁移
②化学需氧量(COD)是重要的水质指标,其数值表示将1L水中的有机物氧化为CO2、H2O所需消耗的氧气的质量.利用微生物燃料电池来处理某些污水并进行发电,如果1L废水中有机物(折算成葡萄糖)氧化所提供的化学能低于5.6kJ,就没有
发电的价值.则适合用微生物燃料电池发电的污水,其COD最低为384mg/L.
(已知葡萄糖的燃烧热为2800kJ/mol)
I.工业上利用废铁屑(含少量氧化铝、氧化铁等)生产碱式硫酸铁的工艺流程如图1:

已知:25℃时部分阳离子以氢氧化物形式沉淀时溶液的pH见表:
| 沉淀物 | Fe(OH)3 | Fe(OH)2 | Al(OH)3 |
| 开始沉淀 | 2.3 | 7.5 | 3.4 |
| 完全沉淀 | 3.2 | 9.0 | 4.4 |
(1)加入少量NaHCO3的目的是调节pH在4.4-7.5范围内,使溶液中Al 3+沉淀.
(2)若沉淀完全时溶液中金属离子浓度为1.0×10-5mol/L,则Ksp[Fe(OH)2]=1.0×10-15.
(3)在实际生产中,反应②常同时通入O2以减少NaNO2的用量,若标况下有33.6L O2参与反应,则相当于节约NaNO2的物质的量为6mol.
(4)该生产碱式硫酸铁的工艺过程中存在的明显缺点是会产生一氧化氮,会造成大气污染.
II.微生物燃料电池是以微生物作催化剂,以有机污水为燃料,将有机污水中的化学能直接转化为电能的一种装置.
(5)重庆大学研究出一种微生物燃料电池,可以将污水中的CH3COO-处理掉,
其总反应为:2CH3COOK+4H2O+8K2S2O8═4CO2↑+7H2SO4+9K2SO4,写出该微生物
燃料电池负极的电极反应式CH3COO-+2H2O-8e-=2CO2↑+7H+.
(6)以葡萄糖为燃料的微生物燃料电池结构示意图如图2:
①关于该电池的叙述,正确的有BD
A.电池的正极反应为:O2+2H2O+4e-═4OH-
B.在电池反应中,每消耗90克葡萄糖,经外电路通过的电子数为12NA
C.该电池能够在高温下工作
D.放电过程中,H+从负极区向正极区迁移
②化学需氧量(COD)是重要的水质指标,其数值表示将1L水中的有机物氧化为CO2、H2O所需消耗的氧气的质量.利用微生物燃料电池来处理某些污水并进行发电,如果1L废水中有机物(折算成葡萄糖)氧化所提供的化学能低于5.6kJ,就没有
发电的价值.则适合用微生物燃料电池发电的污水,其COD最低为384mg/L.
(已知葡萄糖的燃烧热为2800kJ/mol)
2.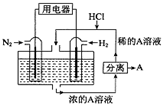 科学家设想以N2和H2为反应物,以溶有A的稀盐酸为电解质溶液,可制造出既能提供电源,又能固氮的新型燃料电池,装置如图所示,下列说法不正确的是( )
科学家设想以N2和H2为反应物,以溶有A的稀盐酸为电解质溶液,可制造出既能提供电源,又能固氮的新型燃料电池,装置如图所示,下列说法不正确的是( )
 科学家设想以N2和H2为反应物,以溶有A的稀盐酸为电解质溶液,可制造出既能提供电源,又能固氮的新型燃料电池,装置如图所示,下列说法不正确的是( )
科学家设想以N2和H2为反应物,以溶有A的稀盐酸为电解质溶液,可制造出既能提供电源,又能固氮的新型燃料电池,装置如图所示,下列说法不正确的是( )| A. | 该电池外电路电流从通入H2的电流流向通入N2的电极 | |
| B. | 反应过程中溶液的pH会变大,故需要加入盐酸 | |
| C. | 通入N2的电极发生的电极反应式为:N2+6e-+8H+═2NH4+ | |
| D. | 通入H2的电极为负极,A为NH4Cl |
19.已知有机化合物A只由C、H两种元素组成且能使溴水褪色,其产量可以用来衡量一个国家石油化工发展水平.A、B、C、D、E有如下关系:则下列推断不正确的是( )
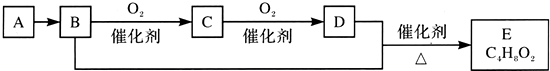

| A. | 鉴别A和甲烷可选择使用酸性高锰酸钾溶液 | |
| B. | D中含有的官能团为羧基,利用D物质可以清除水壶中的水垢 | |
| C. | 物质C的结构简式为CH3CHO,E的名称为乙酸乙酯 | |
| D. | B+D→E的化学方程式为CH3CH2OH+CH3COOH$?_{△}^{催化剂}$CH3COOC2H5 |
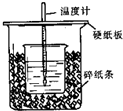 用50mL0.50mol/L盐酸与50mL0.55mol/LNaOH溶液在如图所示的装置中进行中和反应.通过测定反应过程中所放出的热量可计算中和热.回答下列问题:
用50mL0.50mol/L盐酸与50mL0.55mol/LNaOH溶液在如图所示的装置中进行中和反应.通过测定反应过程中所放出的热量可计算中和热.回答下列问题: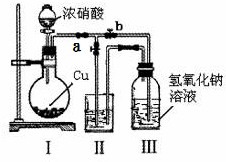 针对网络上流传的隔夜熟肉中因亚硝酸钠(NaNO2)含量严重超标而不能食用的说法,某兴趣小组开展如下探究活动:
针对网络上流传的隔夜熟肉中因亚硝酸钠(NaNO2)含量严重超标而不能食用的说法,某兴趣小组开展如下探究活动: