题目内容
6.CH3COOH分别跟H-18O-C2H5和H-16O-C2H5酯化反应后,两者生成的水分子的相对分子质量( )| A. | 相等 | B. | 前者小 | C. | 前者大 | D. | 不能确定 |
分析 羧酸跟醇的反应过程是:羧酸分子中羧基中的羟基与醇分子中羟基的氢原子结合成水,其余部分互相结合成酯,以此解答该题.
解答 解:羧酸跟醇的反应,羧酸分子中羧基中的羟基与醇分子中羟基的氢原子结合成水.
CH3COOH+H-18O-C2H5$?_{△}^{浓硫酸}$CH3CO18O-C2H5+H20,
CH3COOH+H-16O-C2H5$?_{△}^{浓硫酸}$CH3CO16O-C2H5+H20,
故两者生成的水分子的相对分子质量相等.
故选A.
点评 本题考查酯化反应,侧重于学生的分析能力的考查,难度较小,注意酯化反应原理是酸分子中的羟基与醇分子中羟基的氢原子结合成水.

练习册系列答案
 小学学习好帮手系列答案
小学学习好帮手系列答案 小学同步三练核心密卷系列答案
小学同步三练核心密卷系列答案
相关题目
16.柠檬烯是一种食用香料,其结构简式如图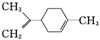 所示.有关柠檬烯的分析正确的是( )
所示.有关柠檬烯的分析正确的是( )
 所示.有关柠檬烯的分析正确的是( )
所示.有关柠檬烯的分析正确的是( )| A. | 它的一氯代物有6种 | |
| B. | 一定条件下,它分别可以发生加成、取代、氧化等反应 | |
| C. | 它的分子中所有的碳原子可能在同一平面上 | |
| D. | 它和丁基苯(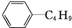 )互为同分异构体 )互为同分异构体 |
14.将固体NH4Br置于密闭容器中,在某温度下,发生下列反应:NH4Br(s)═NH3(g)+HBr(g),2HBr(g)?Br2(g)+H2(g).2min时,测知H2的浓度为0.5mol•L-1,HBr的浓度为4mol•L-1,若上述反应速率用v(NH3)表示,下列速率正确的是( )
| A. | 0.5mol•L-1•min-1 | B. | 2.5mol•L-1•min-1 | ||
| C. | 2mol•L-1•min-1 | D. | 5mol•L-1•min-1 |
18.已知反应如下:N2(g)+3H2(g)?2NH3(g),在某条件下一定量的N2 和一定量的H2反应生成4mol NH3时放出的热量为184.0kJ,将相同条件下的1mol N2 和3mol H2 放在一密闭容器中进行充分反应,测得反应放出的热量为( )
| A. | 一定大于92.0 kJ | B. | 一定等于92.0 kJ | C. | 一定小于92.0 kJ | D. | 不能确定 |
16.下列有关说法正确的是( )
| A. | 硫酸工业中二氧化硫的催化氧化,不采用高压是因为压强对SO2转化率无影响 | |
| B. | 同温、同浓度的盐酸和氢氧化钠稀溶液中,水的电离程度相同 | |
| C. | 3C(s)+CaO(s)═CaC2(s)+CO(g)在常温下不能自发进行,说明该反应的△H>0 | |
| D. | 合成氨时,其他条件不变升高温度,反应速率v(H2)和氢气的平衡转化率均增大 |

 ,A的结构简式
,A的结构简式 .
. .
. .
.