题目内容
下列叙述正确的是( )
| A、固体氯化钠不导电,所以氯化钠不是电解质 |
| B、虽然NaHSO4溶于水能电离出H+,但它不是酸 |
| C、“纳米材料”是粒子直径1~100 nm的材料,它属于胶体 |
| D、在一个氧化还原反应中,有一种元素被氧化肯定有另一种元素被还原 |
考点:电解质与非电解质,酸、碱、盐、氧化物的概念及其相互联系,分散系、胶体与溶液的概念及关系
专题:
分析:电解质是在水溶液里或熔融状态下能导电的化合物,非电解质是在水溶液里或熔融状态下都不能导电的化合物,单质和混合物既不是电解质,也不是非电解质.物质能导电必须存在能自由移动的带电微粒.
解答:
解:A、固态氯化钠不导电,但在水溶液或熔融状态下能导电,属于电解质,故A错误;
B、溶于水电离出氢离子的化合物不一定是酸,硫酸氢钠是酸式盐,故B正确;
C、纳米粒子直径为l~100nm之间,所形成的分散系为胶体分散系,故C错误;
D、氧化还原反应中,可能同种元素既被氧化也被还原,故D错误,故选B.
B、溶于水电离出氢离子的化合物不一定是酸,硫酸氢钠是酸式盐,故B正确;
C、纳米粒子直径为l~100nm之间,所形成的分散系为胶体分散系,故C错误;
D、氧化还原反应中,可能同种元素既被氧化也被还原,故D错误,故选B.
点评:本题主要考查的是电解质、酸碱盐的定义、分散系、氧化还原反应等,难度不大,综合性较强.

练习册系列答案
相关题目
下列有关实验装置(部分夹持装置已省略)进行的相应实验,能达到实验目的是( )
A、 用图所示装置可制取Cl2 |
B、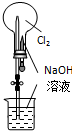 用图所示装置可完成“喷泉”实验 |
C、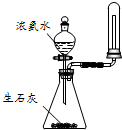 用图所示装置可制取并收集干燥纯净的NH3 |
D、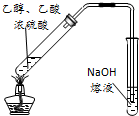 用图所示装置可用于实验室制取乙酸乙酯 |
配制一定物质的量浓度的NaOH溶液时,造成所配溶液浓度偏高的原因是( )
| A、所用NaOH已吸潮 |
| B、容量瓶未干燥 |
| C、烧杯内有少量NaOH溶液残留 |
| D、定容时俯视液面 |
下列高分子材料中属于线性结构的是( )
| A、聚丙烯 | B、硫化橡胶 |
| C、电木 | D、有机玻璃 |
下列关于Na2CO3和NaHCO3的是( )
| A、与足量酸反应:离子方程式相同 |
| B、热稳定性:Na2CO3<NaHCO3 |
| C、常温下在水中的溶解度:Na2CO3>NaHCO3 |
| D、等质量的碳酸钠和碳酸氢钠与足量酸反应产生CO2的质量:Na2CO3<NaHCO3 |
某无色透明溶液中能大量共存的离子组是( )
| A、Na+、Al3+、HCO3-、NO3- |
| B、AlO2-、Mg2+、H+、K+ |
| C、NH4+、Na+、CH3COO-、NO3- |
| D、Na+、NO3-、ClO-、I- |
 醇脱水是合成烯烃的常用方法,实验室合成环己烯的反应和实验装置如图:
醇脱水是合成烯烃的常用方法,实验室合成环己烯的反应和实验装置如图: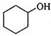
 +H2O
+H2O