题目内容
8.某温度时,水的离子积常数KW=10-13,将此温度下pH=11的Ba(OH)2溶液aL与pH=1的H2SO4溶液bL混合.设混合溶液体积为两者之和,所得固体体积忽略不计.若所得混合溶液为中性,则a:b=10:1.分析 所得混合溶液为中性,一定满足n(H+)=n(OH-),该温度下水的离子积常数KW=10-13,则pH=11的溶液中c(OH-)=$\frac{1{0}^{-13}}{1{0}^{-11}}$=0.01mol/L,pH=1的硫酸中氢离子浓度为:0.1mol/L,据此列式计算.
解答 解:所得混合溶液为中性,则n(H+)=n(OH-),该温度下水的离子积常数KW=10-13,则pH=11的溶液中c(OH-)=$\frac{1{0}^{-13}}{1{0}^{-11}}$=0.01mol/L,
pH=1的硫酸中氢离子浓度为:0.1mol/L,
则:bL×0.1mol/L=aL×0.01mol/L,
解得a:b=10:1,
故答案为:10:1.
点评 本题考查了溶液pH的计算,题目难度不大,明确溶液酸碱性与溶液pH的关系为解答关键,注意本题中水的离子积为KW=10-13,为易错点,试题培养了学生的化学计算能力.

练习册系列答案
相关题目
18.下列物质暴露在空气中,因发生氧化还原反应而变质的是( )
| A. | NaOH | B. | CaO | C. | Na2CO3 | D. | FeSO4 |
19.按混合物、纯净物、强电解质、弱电解质、非电解质的顺序排列正确的是( )
| A. | 盐酸、氯气、硫酸钡、二氧化碳、二氧化硫 | |
| B. | 硫酸、氨水、醋酸、乙醇、二氧化氮 | |
| C. | 漂白粉、胆矾、碳酸钙、醋酸、二氧化碳 | |
| D. | 干冰、氯水、氯化氢、次氯酸、一氧化碳 |
16.常温常压下二氧化碳和过氧化钠反应后得到碳酸钠和氧气,若反应中固体质量增加了28g,反应中有关物质的物理量正确的是(NA表示阿伏加德罗常数)( )
| A. | 参与反应的过氧化钠中含阴离子2 mol | |
| B. | 参与反应的二氧化碳的体积为22.4 L | |
| C. | 反应中电子转移的数目为NA个 | |
| D. | 将生成的碳酸钠溶解在1L水中,能得到1mol/L的碳酸钠溶液 |
3.下列溶液中通入足量CO2,一直没有沉淀生成的是( )
| A. | 氯化钙溶液 | B. | 饱和碳酸钠溶液 | C. | 硅酸钠溶液 | D. | 澄清石灰水 |
13.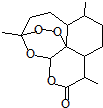 2015年10月5日诺贝尔医学奖授予中国女药学家屠呦呦及美国科学家威廉•坎贝尔和日本大村智,以表彰他们在寄生虫疾病治疗方面取得的成就.屠呦呦1971年发现、分离、提纯并用于治疟新药“青蒿素”,拯救了数千万人的生命.青蒿素分子结构如图.下列说法错误的是( )
2015年10月5日诺贝尔医学奖授予中国女药学家屠呦呦及美国科学家威廉•坎贝尔和日本大村智,以表彰他们在寄生虫疾病治疗方面取得的成就.屠呦呦1971年发现、分离、提纯并用于治疟新药“青蒿素”,拯救了数千万人的生命.青蒿素分子结构如图.下列说法错误的是( )
 2015年10月5日诺贝尔医学奖授予中国女药学家屠呦呦及美国科学家威廉•坎贝尔和日本大村智,以表彰他们在寄生虫疾病治疗方面取得的成就.屠呦呦1971年发现、分离、提纯并用于治疟新药“青蒿素”,拯救了数千万人的生命.青蒿素分子结构如图.下列说法错误的是( )
2015年10月5日诺贝尔医学奖授予中国女药学家屠呦呦及美国科学家威廉•坎贝尔和日本大村智,以表彰他们在寄生虫疾病治疗方面取得的成就.屠呦呦1971年发现、分离、提纯并用于治疟新药“青蒿素”,拯救了数千万人的生命.青蒿素分子结构如图.下列说法错误的是( )| A. | 青蒿素的分子式为C15H22O5 | B. | 青蒿素是芳香族化合物 | ||
| C. | 青蒿素可以发生水解反应 | D. | 青蒿素不能使酸性KMnO4溶液褪色 |
20.科学家指出,食用虾类等水生甲壳类动物的同时服用维生素C容易中毒,这是因为对人体无害的+5价砷类物质在维生素C的作用下,能够转化为有毒的+3价砷类化合物.下列说法不正确的是( )
| A. | 维生素C具有还原性 | |
| B. | 上述过程中砷元素发生还原反应 | |
| C. | 上述过程中+5价砷类物质作氧化剂 | |
| D. | 上述过程中+3价砷类化合物是氧化产物 |
18.下列化合物的核磁共振氢谱中出现三组峰的是( )
| A. | 甲苯 | B. | 2,4-二甲基戊烷 | ||
| C. | 丙三醇 | D. | 2,4,6-三硝基甲苯 |