题目内容
3.下列实验或操作方法正确的是( )| A. | 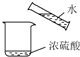 稀释浓硫酸 | B. | 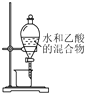 分离水和乙酸 | C. | 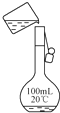 转移溶液 | D. | 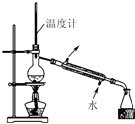 制取蒸馏水 制取蒸馏水 |
分析 A.稀释浓硫酸时,必须将浓硫酸倒入水中,且不断用玻璃棒搅拌;
B.互溶且熔沸点差别较大的液体采用蒸馏方法分离,互不相溶的液体采用分液方法分离;
C.向容量瓶中转移溶液时,需要用玻璃棒引流;
D.蒸馏制取蒸馏水时,温度计测量馏分温度,且冷凝管中水流采用“下进上出”原则.
解答 解:A.稀释浓硫酸时,必须将浓硫酸倒入水中,且不断用玻璃棒搅拌,否则易溅出液体而产生安全事故,故A错误;
B.互溶且熔沸点差别较大的液体采用蒸馏方法分离,互不相溶的液体采用分液方法分离,水和乙酸互溶,应该采用蒸馏方法分离,故B错误;
C.向容量瓶中转移溶液时,需要用玻璃棒引流,否则易溅出液体而导致配制溶液浓度偏低,故C错误;
D.蒸馏制取蒸馏水时,温度计测量馏分温度,温度计水银球应该位于蒸馏烧瓶支管口处,且冷凝管中水流采用“下进上出”原则,实验操作正确,故D正确;
故选D.
点评 本题考查化学实验方案评价,为高频考点,明确实验原理及实验基本操作规范性是解本题关键,侧重考查学生实验操作、实验分析判断能力,题目难度不大.

练习册系列答案
相关题目
13.在 100mL 0.10mol•L-1的 AgNO3(aq) 中,加入 100mL 溶有 2.08g BaCl2 的溶液,再加入 100mL 溶有 2.50g CuSO4•5H2O 的溶液,充分反应.下列说法中正确的是( )
| A. | 最终得到白色沉淀和无色溶液 | |
| B. | 最终得到的白色沉淀是等物质的量的两种化合物的混合物 | |
| C. | 混合过程中,逸出无色气体 | |
| D. | 在最终得到的溶液中,c(Cu2+)=0.01 mol•L-1 |
14.甲、乙两种固体的溶解度曲线如图所示.下列说法中,不正确的是( )
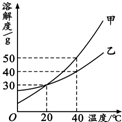

| A. | 20℃时,甲溶液中溶质的质量分数一定等于乙溶液中溶质的质量分数 | |
| B. | 40℃时,分别在100 g水中加入40 g甲、乙,所得溶液溶质的质量分数相等 | |
| C. | 40℃时,分别在100 g水中加入30 g甲、乙,同时降温至20℃,甲、乙溶液均为饱和溶液 | |
| D. | 20℃时,分别在100 g水中加入40 g甲、乙,加热到40℃时,乙溶液为饱和溶液 |
18.2015年巴黎气候变化大会规定:本世纪实现温室气体净零排放.下列物质燃烧时能实现二氧化碳零排放的是( )
| A. | 天然气 | B. | 氢气 | C. | 水煤气 | D. | 煤炭 |
8.下列有关物质用途的描述不正确的是( )
| A. | 氧化铁可制作防锈油漆 | |
| B. | 碳酸氢钠可制作焙制糕点的发酵粉 | |
| C. | 氯气不能用来合成药物,因为它有毒 | |
| D. | NO能促进血管扩张,防止血管栓塞 |
12.下列变化中属于化学变化的是( )
| A. | 由于冰得到二氧化碳气体 | |
| B. | 胆矾加热失去结晶水 | |
| C. | 烧瓶中盛有二氧化氮气体,加入活性炭后,红棕色逐渐消失 | |
| D. | 铜导电. |
2.把7.2g铁粉投入40ml某浓度的硝酸中,充分反应后剩余固体1.6g,产生NO2和NO的混合气体0.08mol.若不考虑N2O4的存在,则该硝酸的物质的量浓度为( )
| A. | 3.5mol•L-1 | B. | 7.0mol•L-1 | C. | 4.5mol•L-1 | D. | 9.0mol•L-1 |