题目内容
今有1.40 g碱金属(M)及其氧化物(M2O)的混合物与水反应,生成1.79 g碱。求混合物成分及其质量。
混合物为K、K2O;K 0.498 g,K2O 0.902 g
解析:设碱金属M的相对原子质量为x,则:
2M+2H2O====2MOH+H2↑
M2O+H2O====2MOH
(1)若1.40 g全为碱金属,则产生的MOH的质量为![]() g;
g;
(2)若1.40 g全为氧化物,则产生MOH的质量为![]() ,显然有
,显然有![]() <1.79
<1.79
<![]() 。
。
解得24.3<x<61.03,只有钾才适合此条件。设a和b分别为钾及氧化钾的质量,则:
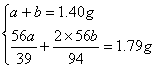
解得![]()
混合物为钾和氧化钾;钾为0.498 g,氧化钾为0.902 g。

练习册系列答案
 亮点激活精编提优100分大试卷系列答案
亮点激活精编提优100分大试卷系列答案 智趣寒假作业云南科技出版社系列答案
智趣寒假作业云南科技出版社系列答案
相关题目