题目内容
将下列物质按酸、碱、盐分类排列,正确的是( )
| A、硫酸、纯碱、CaSO4 |
| B、HCl、烧碱、CuSO4 |
| C、HNO3、乙醇、氯化钠 |
| D、碳酸、CaO、苛性钠 |
考点:酸、碱、盐、氧化物的概念及其相互联系
专题:物质的分类专题
分析:A、纯碱不是碱;
B、根据酸碱盐的概念来分析;
C、乙醇不是碱;
D、氧化钙不是碱,苛性钠不是盐.
B、根据酸碱盐的概念来分析;
C、乙醇不是碱;
D、氧化钙不是碱,苛性钠不是盐.
解答:
解:酸的定义:电离出的阳离子全部是氢离子的化合物是酸;碱的定义:电离出阴离子全部是氢氧根的化合物是碱;盐的定义:电离出的阳离子是金属离子或铵根离子,阴离子是酸根离子的化合物.
A、纯碱是Na2CO3,是盐不是碱,故A错误;
B、HCl是酸,烧碱NaOH是碱,CuSO4是盐,故B正确;
C、乙醇不是碱,故C错误;
D、CaO是氧化物而不是碱,苛性钠NaOH是碱而不是盐,故D错误.
故选B.
A、纯碱是Na2CO3,是盐不是碱,故A错误;
B、HCl是酸,烧碱NaOH是碱,CuSO4是盐,故B正确;
C、乙醇不是碱,故C错误;
D、CaO是氧化物而不是碱,苛性钠NaOH是碱而不是盐,故D错误.
故选B.
点评:本题在考查物质分类的基础上考查了酸碱盐的概念,属于基础型题目,难度不大.

练习册系列答案
相关题目
X、Y、Z、R、W五种元素的原子序数依次增大且不大于20,其中Y与W、X与Z分别为同族元素.原子半径X<Y<W<R<Z,W原子的最外层电子数与K层电子数两倍的和等于内层电子总数,Y、W核外电子数之和与Z、R的核外电子数之和相等.下列说法正确的是( )
| A、Y、Z形成的化合物中不可能存在共价键 |
| B、由X、Y、R形成的化合物与X、Y、Z形成的化合物能发生反应生成盐 |
| C、工业上通常用焦炭高温下还原的方法获得Z、R的单质 |
| D、把少量W与R形成的化合物加入水中能迅速溶解得到一种无色透明的溶液 |
已知两种弱酸的酸性:HA>HB,在常温下下列各项比较中正确的是( )
| A、等物质的量浓度的HA溶液与NaB溶液等体积的混合液中:2c(Na+)═c(A-)+c(B-)+c(HA)+c(HB) |
| B、pH相等的NaA与KB两溶液中:[c(Na+)-c(A-)]<[c(K+)-c(B-)] |
| C、pH=9的三种溶液 ①NaB ②NH3?H2O ③NaOH中由水电离出的c(OH-):①>②>③ |
| D、两种溶液①0.1mol/L HA溶液 ②0.1mol/L HB溶液,加水稀释至pH 相同,需加水的量前者小于后者 |
下列物质既能使酸性高锰酸钾溶液褪色,又能使溴水褪色的是( )
| A、甲烷 | B、乙烯 | C、苯 | D、乙酸乙酯 |
化学与社会、生活密切相关,下列有关说法不正确的是( )
| A、利用清洁能源代替化石燃料,有利于节约资源、保护环境 |
| B、食品添加剂苯甲酸钠,它是苯的一种同系物所对应的钠盐 |
| C、抗酸药的种类很多,如碳酸氢钠、碳酸钙、碳酸镁、氢氧化铝、等 |
| D、乙醇属于可再生能源 |
用如图装置电解硫酸钾溶液制取氢气,氧气,硫酸和氢氧化钾.从开始通电时,收集B和C逸出的气体.1min后测得B口的气体体积为C口处的一半,下列说法不正确的是( )

| A、电源左极为正极 |
| B、电解槽左侧的电极反应方程式为:2H2O-4e-═O2+4H+ |
| C、D口导出的溶液为KOH溶液,且浓度比刚加入电解槽右侧时的浓度大 |
| D、在标准状况下,若1min后从C口处收集到的气体比B口处收集到的气体多2.24L,则有0.1NA个SO42-通过阴离子膜 |
NA为阿伏伽德罗常数的值.下列叙述正确的是( )
| A、标准状态下,22.4L水中含有的氧原子数为NA |
| B、常温常压下,8gO2含有4 NA个电子 |
| C、25℃时,pH=13的1L Ba(OH)2溶液中含有OH-的数目为0.2NA |
| D、53.5gNH4Cl中含有H-Cl键的个数为4NA |
下列离子方程式书写错误的是( )
| A、铝粉投入到NaOH溶液中:2Al+2OH-=2AlO2-+H2↑ |
| B、Al(OH)3溶于NaOH溶液中:Al(OH)3+OH-=AlO2-+2H2O |
| C、Ca(OH)2溶液中通入足量的CO2:CO2+OH-=HCO3- |
| D、Al2O3粉末溶于NaOH溶液中:Al2O3+2OH-=2AlO2-+H2O |
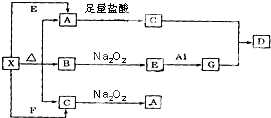 如图表示的反应关系中,部分产物被略去.已知白色固体粉末X受热分解,恢复到室温生成白色固体A,无色液体B,无色气体C.X、E、G的焰色反应均为黄色,D为白色沉淀.
如图表示的反应关系中,部分产物被略去.已知白色固体粉末X受热分解,恢复到室温生成白色固体A,无色液体B,无色气体C.X、E、G的焰色反应均为黄色,D为白色沉淀.