题目内容
(9分)超氧化钾(KO2)又称为化学氧自救剂,容易与空气中的水、二氧化碳等发生反应,主要用于煤矿井下急救。某兴趣小组拟选用如下装置制备超氧化钾(部分夹持仪器已略去)。
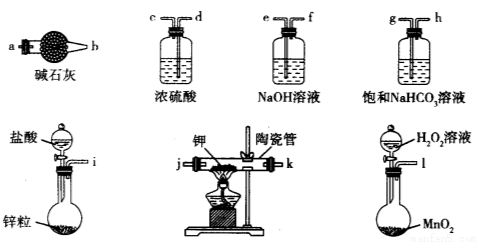
请回答下列问题:
(1)请选择必要的装置,按气流方向的连接顺序为____________________(填仪器接口的字母)。
(2)请根据完整的实验装置,完成下列实验步骤:①_____________________;②装入药品,打开分液漏斗活塞;③持续通入气体一段时间后,点燃酒精灯进行反应;④反应结束后,熄灭酒精灯,待反应管冷却至室温,停止通入氧气,并关闭分液漏斗的活塞;⑤拆除装置,取出产物。
(3)数据记录如下:

根据数据计算可得实验式KOx,则x=____________________。
(4)超氧化钾可吸收二氧化碳,并生成氧气,因此可以作为飞船、潜艇等密闭系统的氧气再生剂。写出超氧化钾与二氧化碳反应的化学方程式:____________________________________。与过氧化钠相比,其优点是____________________________________。
(1)l e f d c j k a(j k可互换)或者l d c j k a(j k可互换); (2)检查装置的气密性;(3)1.75;
(4)4KO2 + 2CO2=2K2CO3 + 3O2↑(2分)
相同质量的过氧化钠和超氧化钾相比,KO2释放的O2更多。
【解析】
试题分析:(1)制取KO2的反应方程式是:K+O2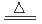 KO2,所以制取KO2的步骤应该是制取氧气、除去杂质、干燥气体、制取KO2、防止反应的装置,因此装置的连接顺序是:l e f d c j k a;(2)实验步骤①检查装置的气密性;②装入药品,打开分液漏斗活塞;③持续通入气体一段时间后,点燃酒精灯进行反应;④反应结束后,熄灭酒精灯,待反应管冷却至室温,停止通入氧气,并关闭分液漏斗的活塞;⑤拆除装置,取出产物。(3)n(K)=(15.19g-14.80g)÷39g/mol=0.01mol,n(O)= (15.47g-15.19g) ÷16g/mol= 0.0175mol,所以n(O):n(K)= 0.0175mol: 0.01mol=1.75;(4) 超氧化钾与二氧化碳反应的化学方程式:4KO2 + 2CO2=2K2CO3 + 3O2↑; 与过氧化钠相比,其优点是相同质量的过氧化钠和超氧化钾相比,KO2释放的O2更多。
KO2,所以制取KO2的步骤应该是制取氧气、除去杂质、干燥气体、制取KO2、防止反应的装置,因此装置的连接顺序是:l e f d c j k a;(2)实验步骤①检查装置的气密性;②装入药品,打开分液漏斗活塞;③持续通入气体一段时间后,点燃酒精灯进行反应;④反应结束后,熄灭酒精灯,待反应管冷却至室温,停止通入氧气,并关闭分液漏斗的活塞;⑤拆除装置,取出产物。(3)n(K)=(15.19g-14.80g)÷39g/mol=0.01mol,n(O)= (15.47g-15.19g) ÷16g/mol= 0.0175mol,所以n(O):n(K)= 0.0175mol: 0.01mol=1.75;(4) 超氧化钾与二氧化碳反应的化学方程式:4KO2 + 2CO2=2K2CO3 + 3O2↑; 与过氧化钠相比,其优点是相同质量的过氧化钠和超氧化钾相比,KO2释放的O2更多。
考点:考查制取KO2的装置的连接、操作方法、制取原理、性能的比较的知识。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案 C、
C、 C、
C、 C ⑥同系物:CH2O2、C2H4O2、C3H6O2、C4H8O2
C ⑥同系物:CH2O2、C2H4O2、C3H6O2、C4H8O2 CaSiO3+CO2↑的发生,说明硅酸的酸性强于碳酸
CaSiO3+CO2↑的发生,说明硅酸的酸性强于碳酸
