题目内容
 三氟化氮(NF3)是一种无色、无味、无毒且不可燃的气体,在半导体加工、太阳能电池制造和液晶显示器制造中得到广泛应用.它可在铜的催化作用下由F2和过量的NH3反应得到,该反应另一种产物为盐.
三氟化氮(NF3)是一种无色、无味、无毒且不可燃的气体,在半导体加工、太阳能电池制造和液晶显示器制造中得到广泛应用.它可在铜的催化作用下由F2和过量的NH3反应得到,该反应另一种产物为盐.(1)该反应的化学方程式为
(2)N、F两种元素的氢化物稳定性比较,NH3
(3)N3-被称为类卤离子,写出1种与N3-互为等电子体的分子的化学式
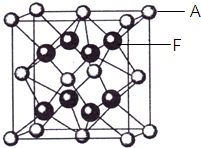
(4)元素A基态原子的核外电子排布式为1s22s22p63s23p64s2,A跟氟可形成离子化合物,其晶胞结构如图,该离子化合物的化学式为
(5)化合物AF2的晶胞结构如图所示,该离子化合协晶体的密度为a g/cm3,则晶胞的体积是
考点:晶胞的计算,位置结构性质的相互关系应用
专题:元素周期律与元素周期表专题,化学键与晶体结构
分析:(1)F2和过量的NH3反应生成NF3和NH4F,根据分子中δ键和孤电子对数判断杂化类型和分子的空间构型;
(2)元素的非金属性越强,对应的氢化物越稳定;
(3)N3-含有3个原子和22个电子,结合等电子体的定义分析;
(4)元素A基态原子的核外电子排布式为1s22s22p63s23p64s2,应为Ca元素,利用均摊法计算化学式;
(5)根据晶胞计算AF2个数,进而计算质量,结合ρ=
计算.
(2)元素的非金属性越强,对应的氢化物越稳定;
(3)N3-含有3个原子和22个电子,结合等电子体的定义分析;
(4)元素A基态原子的核外电子排布式为1s22s22p63s23p64s2,应为Ca元素,利用均摊法计算化学式;
(5)根据晶胞计算AF2个数,进而计算质量,结合ρ=
| m |
| V |
解答:
解:(1)F2和过量的NH3反应生成NF3和NH4F,反应的方程式为3F2+4NH3
NF3+3NH4F,NF3中含有3个δ键,且孤电子对数为
=1,则应为sp3杂化,空间构型为三角锥形,
故答案为:3F2+4NH3
NF3+3NH4F;sp3杂化;三角锥形;
(2)由于非金属性N<F,则HF更稳定,故答案为:<;
(3)N3-含有3个原子和22个电子,价电子总数为16,则对应的等电子体有CO2或CS2、N2O等,故答案为:N2O或CO2;
(4)元素A基态原子的核外电子排布式为1s22s22p63s23p64s2,应为Ca元素,由晶胞结构可知Ca2+离子位于晶胞的定点和面心,共含有8×
+6×
=4个,F-离子位于体心,共8个,则化学式为CaF2,
故答案为:CaF2;
(5)晶胞平均含有4个Ca2+,8个F-,质量为
g,该离子化合协晶体的密度为a g/cm3,则晶胞的体积是
cm3,故答案为:
.
| ||
| 5-3 |
| 2 |
故答案为:3F2+4NH3
| ||
(2)由于非金属性N<F,则HF更稳定,故答案为:<;
(3)N3-含有3个原子和22个电子,价电子总数为16,则对应的等电子体有CO2或CS2、N2O等,故答案为:N2O或CO2;
(4)元素A基态原子的核外电子排布式为1s22s22p63s23p64s2,应为Ca元素,由晶胞结构可知Ca2+离子位于晶胞的定点和面心,共含有8×
| 1 |
| 8 |
| 1 |
| 2 |
故答案为:CaF2;
(5)晶胞平均含有4个Ca2+,8个F-,质量为
| 312 |
| NA |
| 312 |
| aNA |
| 312 |
| aNA |
点评:本题考查较为综合,涉及杂化类型、空间构型、非金属性的比较、等电子体、配合物知识以及晶胞的计算,侧重于知识的掌握与迁移的考查,注意把握晶胞的计算方法,题目难度中等.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
NA代表阿伏加德罗常数,下列说法正确的是( )
| A、0.5 mol Al与足量盐酸反应转移电子数为1.5NA |
| B、标准状况下,11.2 L SO3所含的分子数为0.5NA |
| C、0.1 mol CH4所含的电子数为16NA |
| D、46 g NO2和N2O4的混合物含有的分子数为10NA |
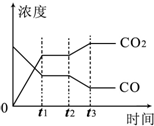 对于反应CO(g)+H2O(g)?H2(g)+CO2(g)
对于反应CO(g)+H2O(g)?H2(g)+CO2(g)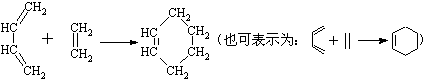

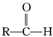 +R′-M′gX→
+R′-M′gX→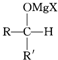
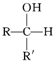 (R,R′均为烃基)
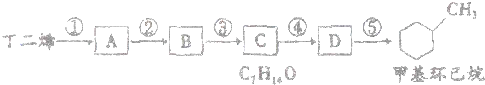
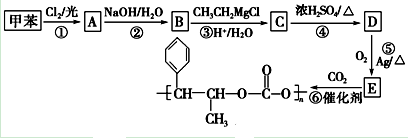
(R,R′均为烃基)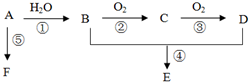 已知A是一种相对分子质量为28的气态烃,它可转化为其他常见有机物,转化关系如图所示.
已知A是一种相对分子质量为28的气态烃,它可转化为其他常见有机物,转化关系如图所示.