题目内容
11. 工业合成气(CO2、CO、H2)在催化剂作用下,于密闭容器中同时存在如下三个反应:
工业合成气(CO2、CO、H2)在催化剂作用下,于密闭容器中同时存在如下三个反应:I CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H1=-58kJ.mol-l
ⅡCO(g)+2H2(g)?CH30H(g)△H2=-99kj.mol-l
ⅢCO(g)+H2O(g)?CO2(g)+H2(g)△H3=-41kJ.mol-l
在压强分别为Pi.P2且起始$\frac{n({H}_{2})}{n(CO)+n(C{O}_{2})}$为一定值条件下,反应体系平衡时CO的转化率(a)与温度关系如图.下列分析正确的是( )
| A. | 由图可知:Pl<P2 | |
| B. | 升高温度反应Ⅱ的平衡常数减小 | |
| C. | 恒压绝热下向反应器中加Ar(g).反应Ⅲ一定不移动 | |
| D. | 其它条件不变,起始时改变CO和CO2比例,平衡时CO转化率不变 |
分析 A.由定一议二原则,当温度一定时,压强Pl时的CO的转化率大;
B.升高温度反应Ⅱ逆向移动,平衡常数减小;
C.恒压绝热下向反应器中加Ar(g),分压减小,平衡向气体体积增大的方向移动;
D.反应Ⅰ生成物水是反应Ⅲ的反应物,起始$\frac{n({H}_{2})}{n(CO)+n(C{O}_{2})}$为一定值,二氧化碳量增加,生成的水增多,CO的转化率增大.
解答 解:A.当温度一定时,压强Pl时的CO的转化率大,平衡正向移动,所以Pl>P2,故A错误;
B.反应Ⅱ正反应为放热反应,升高温度时平衡逆向移动,平衡常数减小,故B正确;
C.恒压绝热下向反应器中加Ar(g),总压强不变,分压减小,平衡向气体体积增大的方向移动,故C错误;
D.起始$\frac{n({H}_{2})}{n(CO)+n(C{O}_{2})}$为一定值,若起始时改变CO和CO2比例,生成的水量会改变,从而影响CO的转化率,故D错误.
故选:B.
点评 本题考查了平衡受温度、压强的影响而移动的问题,注意看准图象是解题的关键,难度中等.

练习册系列答案
 巧学巧练系列答案
巧学巧练系列答案
相关题目
19.在100g浓度为ω%的稀硫酸中加入4g氧化铜粉末,待氧化铜全部溶解后,向所得蓝色溶液中加入10g铁粉,充分反应后,过滤,得滤液和4.8g滤渣.下列计算结果正确的是( )
| A. | 4.8g滤渣是由3.2g铜和1.6g铁组成 | B. | ω=14.7 | ||
| C. | 反应过程中产生的氢气是2.24L | D. | 滤液是20.88%的硫酸亚铁溶液 |
6.由分类思想,下列说法正确的是( )
| A. | 氢氧化钠、盐酸都为强电解质 | |
| B. | 铁生锈、食物腐败都有氧化反应发生 | |
| C. | 糖类、蛋白质都为高分子化合物 | |
| D. | 一氯甲烷、二氧化碳都是极性分子 |
16.下列有关实验操作的说法正确的是( )
| A. | 可用25mL碱式滴定管量取20.00mL KMnO4溶液 | |
| B. | 用pH试纸测定溶液的pH时,需先用蒸馏水润湿试纸 | |
| C. | 将金属钠在研钵中研成粉末,使钠与水反应的实验更安全 | |
| D. | 蒸馏时蒸馏烧瓶中液体的体积不能超过容积的$\frac{2}{3}$,液体也不能蒸干 |
3.模拟电渗析法将海水淡化的工作原理示意图如下.已知X、Y均为惰性电极,模拟海水中富含Na+、Cl-、Ca2+、Mg2+、SO42-、HCO3-等离子.下列叙述中正确的是( )


| A. | M是阴离子交换膜 | B. | Y电极上产生无色气体 | ||
| C. | X电极区域可产生Mg(OH)2 | D. | X电极反应式为4OH--4e-═O2↑+2H2O |
20.NA代表阿伏加德罗常数的值.下列叙述正确的是( )
| A. | 90 g丙醇中存在的共价键总数为15 NA | |
| B. | 1 mol的羟基与1 mol的氢氧根离子所含电子数均为9 NA | |
| C. | 过氧化钠与水反应时,生成0.1 mol O2转移的电子数为0.2 NA | |
| D. | 2 L 0.5 mol/L亚硫酸溶液中含有的H+离子数为2 NA |
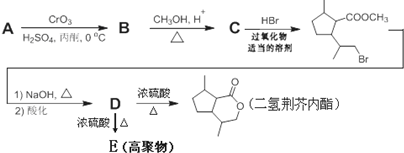
 ,B含有的非氧官能团的名称碳碳双键.C与HBr发生的反应类型是加成反应.
,B含有的非氧官能团的名称碳碳双键.C与HBr发生的反应类型是加成反应.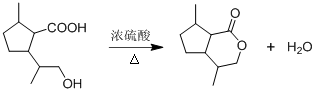 .
. .
. ,其分子中最多有8个碳原子在同一平面上.
,其分子中最多有8个碳原子在同一平面上.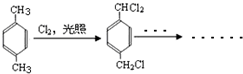
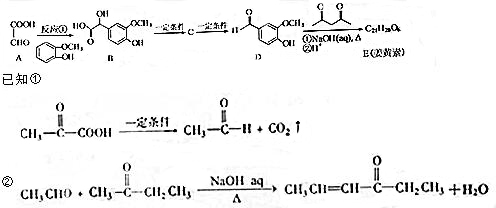
 .
.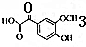 .
.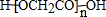 .
. ,下列有关E的叙述正确的是ac.
,下列有关E的叙述正确的是ac.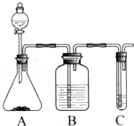 Ⅰ.实验室常用如图中的装置制备乙炔并检验乙炔的性质:
Ⅰ.实验室常用如图中的装置制备乙炔并检验乙炔的性质: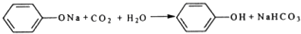 ;
;