题目内容
7.一定条件下,用甲烷可以消除氮的氧化物(NOx)的污染.已知:①CH4(g)+4NO2 (g)═4NO(g)+CO2 (g)+2H2 O(g)△H1=-574kJ•mol-1
②CH4 (g)+4NO(g)═2N2 (g)+CO2 (g)+2H2 O(g)△H2=-1160kJ•mol-1
下列选项不正确的是( )
| A. | CH4 (g)+2NO2 (g)═N2 (g)+CO2 (g)+2H2 O(g)△H=-867 kJ•mol-1 | |
| B. | CH4 (g)+4NO2 (g)═4NO(g)+CO2 (g)+2H2O(l)△H3<△H1 | |
| C. | 若用0.2 mol CH4还原NO2至N2,则反应中放出的热量一定为173.4kJ | |
| D. | 若用标准状况下2.24 L CH4还原NO2至N2,整个过程中转移的电子为0.8mol |
分析 A.由盖斯定律可知,$\frac{①+②}{2}$可得到反应CH4 ( g )+2NO2 ( g )=N2( g )+CO2 ( g )+2H2O (g);
B.氮气再转化为NO的过程是放热过程,水蒸气转化为液态的水是放热过程;
C.利用热化学反应方程式中化学计量数与反应热的关系来计算;
D.利用n=$\frac{V}{Vm}$计算甲烷的物质的量,再利用碳元素化合价的变化来计算转移的电子数.
解答 解:A.反应①+②可得到2CH4(g)+4NO2(g)═2N2(g)+2CO2(g)+4H2O( g ),△H=(-574kJ•mol-1)+(-1160kJ•mol-1)=-1734kJ•mol-1,
则CH4(g)+2NO2(g)═N2(g)+CO2(g)+2H2O( g )△H=-867kJ•mol-1,故A正确;
B.根据CH4(g)+2NO2(g)═N2(g)+CO2(g)+2H2O( g )△H=-867kJ•mol-1,氮气再转化为NO的过程是放热过程,水蒸气转化为液态的水是放热过程,所以CH4 (g)+4NO2 (g)═4NO(g)+CO2 (g)+2H2O(l)△H3<△H1故B正确;
C.由CH4(g)+2NO2(g)═N2(g)+CO2(g)+2H2O( g )△H=-867kJ•mol-1,用0.2 mol CH4还原NO2至N2,放出的热量为0.2mol×867kJ•mol-1=173.4kJ,但是甲烷的反应不一定彻底,故C错误;
D.甲烷的物质的量为0.1mol,碳元素的化合价由-4价升高为+4价,则转移的电子总数为为0.1mol×8=0.8mol,故D正确;
故选C.
点评 本题考查学生利用盖斯定律来计算反应的反应热,并学会利用化学计量数与反应热的关系、利用化合价的变化分析电子转移的数目来就解答即可,题目难度中等.

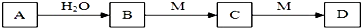
| A. | 若M为具有臭鸡蛋气味的气体,则D可能为酸式盐,且M(A)=M(C) | |
| B. | 若M为铁,则向D的溶液中通入A可能得C | |
| C. | 若C为纯碱,C转化为D的反应是CO32-+H2O+CO2═2HCO3-,则A可能为氯气 | |
| D. | 若M为可溶性铝盐,则A与水反应可能产生氢气,也可能产生氧气 |
| A. | 0.1mol•L-1NaHCO3溶液中:c(Na+)+c(H+)=c(HCO3-)+2c(CO32-)+c(OH-) | |
| B. | 等体积、等物质的量浓度的NaX和弱酸HX混合后呈酸性的溶液中:c(X-)>c(Na+)>c(HX)>c(H+)>c(OH-) | |
| C. | 将0.2 mol•L-1 NaA溶液和0.1 mol•L-1盐酸等体积混合所得碱性溶液中:c(Na+)+c(H+)=c(A-)+c(Cl-)+c(OH-) | |
| D. | 1.5 L 0.1 mol•L-1 NaOH溶液中缓慢通入CO2至溶液增重4.4 g时,溶液中:c(Na+)>c(CO32-)>c(HCO3-)>c(OH-)>c(H+) |
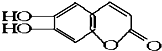 ,具有抗菌作用.若1mol 七叶树内酯,分别与 浓溴水和NaOH溶液完全反应,则消耗的Br2和NaOH的物质的量分别为 ( )
,具有抗菌作用.若1mol 七叶树内酯,分别与 浓溴水和NaOH溶液完全反应,则消耗的Br2和NaOH的物质的量分别为 ( )| A. | 3mol Br2;2mol NaOH | B. | 3mol Br2;4mol NaOH | ||
| C. | 2mol Br2;3mol NaOH | D. | 4mol Br2;4mol NaOH |
| A. | CuSO4 NaCl | B. | NaHCO3 H2SO4 | ||
| C. | AlCl3 氨水 | D. | NaAlO2 HCl |
| A. | 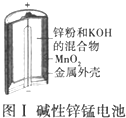 图Ⅰ所示电池中,MnO2的作用是催化剂 | |
| B. | 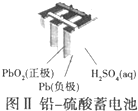 图Ⅱ所示电池工作时,负极质量减轻 | |
| C. | 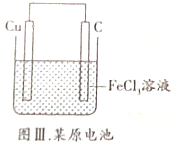 图Ⅲ所示装置工作过程中,Cu作正极 | |
| D. | 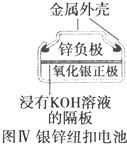 图Ⅳ所示电池为一次电池 |
| A. | 30mL 3mol•Lˉ1的X溶液 | B. | 40mL 2mol•Lˉ1的X溶液 | ||
| C. | 20mL 4mol•Lˉ1的X溶液 | D. | 10mL 5mol•Lˉ1的X溶液 |