题目内容
14.下列实验能达到目的是( )| A. | 只滴加氨水鉴别NaCl、AlCl3、MgCl2、Na2SO4四种溶液 | |
| B. | 用澄清石灰水鉴别Na2CO3、NaHCO3两种溶液 | |
| C. | 用萃取分液的方法除去酒精中的水 | |
| D. | 用可见光束照射以区别溶液和胶体 |
分析 A.氨水与氯化钠、硫酸钠不反应;
B.澄清石灰水与Na2CO3溶液和NaHCO3溶液反应均生成白色沉淀;
C.酒精和水混溶;
D.胶体具有丁达尔现象区别于溶液.
解答 解:A.氨水与氯化钠、硫酸钠不反应,与AlCl3、MgCl2反应生成白色沉淀,故A错误;
B.澄清石灰水与Na2CO3溶液和NaHCO3溶液反应均生成白色沉淀,现象相同,不能鉴别,故B错误;
C.酒精和水混溶不能分层,不能萃取分液,故C错误;
D.胶体具有丁达尔现象区别于溶液,用可见光束照射以区别溶液和胶体,故D正确.
故选D.
点评 本题考查化学实验方案的评价,为高频考点,把握物质的性质、发生的反应为解答的关键,侧重元素化合物知识、物质鉴别及反应现象的考查,题目难度不大.

练习册系列答案
 世纪百通期末金卷系列答案
世纪百通期末金卷系列答案
相关题目
4.下列对有关化学反应过程或实验现象的解释正确的是( )
| A. | Cl2的水溶液可以导电,说明Cl2是电解质 | |
| B. | 某溶液中加入硝酸酸化的氯化钡溶液有白色沉淀生成说明溶液中一定含有SO42- | |
| C. | 向淀粉碘化钾的溶液中加入氯水,溶液变为蓝色,说明Cl2的氧化性强于I2 | |
| D. | 切开金属钠暴露在空气中,光亮表面逐渐变暗2Na+O2=Na2O2 |
2.下列氧化物不能与铝粉发生铝热反应的是( )
| A. | Cr2O3 | B. | MnO2 | C. | WO3 | D. | MgO |
6.科学家研制多种新型杀虫剂代替DDT,化合物A是其中的一种,下列关于化合物A的说法正确的是( )

| A. | 可与FeCl3溶液发生显色反应 | |
| B. | 分子中最少有4个碳原子共平面 | |
| C. | 能发生取代反应和银镜反应 | |
| D. | 与H2完全加成的物质的量之比为1:1 |
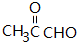 .
.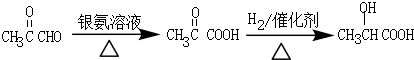 .
.
