题目内容
下列反应的离子方程式正确的是( )
A、苯酚与碳酸钠溶液的反应 |
| B、等体积、等浓度的Ca(HCO3)2和NaOH溶液混合Ca2++2HCO3-+2OH-→CaCO3↓+CO32-+2H20 |
| C、硫化亚铁溶于稀硝酸中:FeS+2H+=Fe2++H2S↑ |
| D、淀粉碘化钾溶液在空气中变蓝2I-+O2+H2O=I2+2OH- |
考点:离子方程式的书写
专题:离子反应专题
分析:A.苯酚酸性大于碳酸氢根离子,所以苯酚能够与碳酸钠溶液反应生成碳酸氢根离子;
B.碳酸氢钙与氢氧化钠的物质的量相等,氢氧根离子不足,离子方程式按照氢氧化钠的化学式组成书写;
C.硫离子和亚铁离子都会被稀硝酸氧化,反应不会生成硫化氢气体;
D.根据电子守恒、质量守恒定律判断.
B.碳酸氢钙与氢氧化钠的物质的量相等,氢氧根离子不足,离子方程式按照氢氧化钠的化学式组成书写;
C.硫离子和亚铁离子都会被稀硝酸氧化,反应不会生成硫化氢气体;
D.根据电子守恒、质量守恒定律判断.
解答:
解:A.苯酚酸性大于碳酸氢根离子,苯酚与碳酸钠溶液的反应离子方程式为: ,故A正确;
,故A正确;
B.等体积、等浓度的Ca(HCO3)2和NaOH溶液混合,二者物质的量相等,反应生成碳酸钙、碳酸氢钠和水,正确的离子方程式为:Ca2++HCO3-+OH-=CaCO3↓+H20,故B错误;
C.硫化亚铁溶于稀硝酸中,反应生成铁离子、硫单质、NO气体和水,正确的离子方程式为:NO3-+FeS+4H+=Fe3++S+NO↑+2H2O,故C错误;
D.淀粉碘化钾溶液在空气中变蓝,碘离子被氧气氧化成碘单质,正确的离子方程式为:4I-+O2+2H2O=2I2+4OH-,故D错误;
故选A.
 ,故A正确;
,故A正确;B.等体积、等浓度的Ca(HCO3)2和NaOH溶液混合,二者物质的量相等,反应生成碳酸钙、碳酸氢钠和水,正确的离子方程式为:Ca2++HCO3-+OH-=CaCO3↓+H20,故B错误;
C.硫化亚铁溶于稀硝酸中,反应生成铁离子、硫单质、NO气体和水,正确的离子方程式为:NO3-+FeS+4H+=Fe3++S+NO↑+2H2O,故C错误;
D.淀粉碘化钾溶液在空气中变蓝,碘离子被氧气氧化成碘单质,正确的离子方程式为:4I-+O2+2H2O=2I2+4OH-,故D错误;
故选A.
点评:本题考查了离子方程式的判断,为中等难度的试题,注意掌握离子方程式的书写原则,明确离子方程式正误判断常用方法:检查反应物、生成物是否正确,检查各物质拆分是否正确,如难溶物、弱电解质等需要保留化学式,检查是否符合守恒关系(如:质量守恒和电荷守恒等)、检查是否符合原化学方程式等

练习册系列答案
 导学全程练创优训练系列答案
导学全程练创优训练系列答案
相关题目
关于下列装置说法正确的是( )
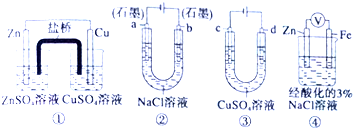

| A、装置①中,盐桥中的K+移向ZnSO4溶液 |
| B、用装置③精炼铜时,c极为粗铜 |
| C、装置②工作一段时间后,a极附近溶液的pH增大 |
| D、装置④中电子Zn流向Fe,装置中有Fe2+生成 |
下列与化学反应能量变化相关的叙述正确的是( )
| A、同温同压下,H2(g)+Cl2(g)═2HCl(g)在光照和点燃条件的△H不同 |
| B、相同条件下2mol氢原子所具有的能量小于1 mol氢分子所具有的能量 |
| C、应用盖斯定律,可以计算某些难以直接测量的反应焓变 |
| D、反应NH3(g)+HCl(g)═NH4Cl(s)在室温下可自发进行:则该反应的△H>0 |
下列化学及实验用语书写正确的是( )
| A、崔化剂 | B、椎形瓶 |
| C、蒸发皿 | D、粹取 |
下列关于电解质溶液的正确判断是( )
| A、由0.1mol/l一元碱HA溶液的pH=3,可推知NaA溶液存在A-+H2O?HA+OH- |
| B、在pH=0的溶液中,Na+、NO3-、SO32-、K+可以大量共存 |
| C、由0.1 mol/l一元碱BOH溶液的pH=10,可推知BOH溶液存在BOH=B++OH- |
| D、在pH=12的溶液中,K+、CL-、HCO3-、Na+可以大量共存 |
下列各溶液中,微粒的物质的量浓度关系或说法不正确的是( )
| A、0.1mol/L Na2CO3溶液:c(OH-)=c(HCO3-)+c(H+)+2c(H2CO3) |
| B、0.1mol/L NH4Cl溶液:c(NH4+)<c(Cl-) |
| C、向醋酸钠溶液中加入适量醋酸,得到的酸性混合溶液:c(Na+)>c(CH3COO-)>c(H+)>c(OH-) |
| D、常温下物质的量浓度相等①NH4HSO4、②(NH4)2SO4、③(NH4)2CO3三种溶液中c(NH4+):①<②<③ |
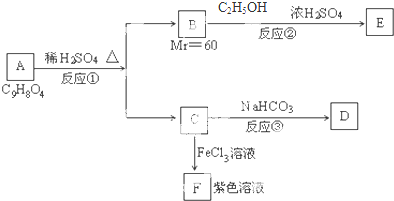 有机物A可发生如下转化:
有机物A可发生如下转化: