题目内容
2. 如图表是元素周期表的一部分,其中a、b、c、d是序号,其它为元素符号.
如图表是元素周期表的一部分,其中a、b、c、d是序号,其它为元素符号.(1)写出B原子结构示意图
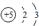 ;
;(2)a和d两元素的原子以共价键
(填化学键类型)形成化合物;
(3)a、b、c三种元素中,原子半径最大的是钠(填元素名称),离子半径最大的是F-(填离子符号);
(4)写出b、c元素各自所形成的最高价氧化物对应的水化物之间发生的反应的离子方程式OH-+Al(OH)3=AlO2-+2H2O;
(5)下列有关图表的叙述中,错误的是BC(选填序号)
A.位于阶梯虚线附近的元素既表现某些金属的性质,又表现某些非金属的性质
B.人们在阶梯虚线附近寻找催化剂
C.元素a的最高价氧化物对应的水化物的酸性是最强的
D.Cs是金属性最强的元素.
分析 表是元素周期表的一部分,其中a、b、c、d是序号,结合位置可知,a为9,b为11,c为13,d为14,对应元素分别为F、Na、Al、Si,B为B,
(1)B的原子序数为5;
(2)Si与F只能以共用电子对成键;
(3)电子层越多,原子半径越大,同周期从左向右原子半径减小,具有相同电子排布的离子中原子序数大的离子半径小;
(4)NaOH和氢氧化铝反应生成偏铝酸钠和水;
(5)A.位于阶梯虚线附近的元素,在金属与非金属的交界处;
B.在过渡元素区寻找催化剂;
C.F无正价;
D.表中Cs的金属性最强.
解答 解:表是元素周期表的一部分,其中a、b、c、d是序号,结合位置可知,a为9,b为11,c为13,d为14,对应元素分别为F、Na、Al、Si,B为B,
(1)B的原子序数为5,原子结构示意图为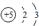 ,故答案为:
,故答案为: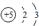 ;
;
(2)Si与F只能以共用电子对成键,二者以共价键结合,故答案为:共价键;
(3)电子层越多,原子半径越大,同周期从左向右原子半径减小,具有相同电子排布的离子中原子序数大的离子半径小,则a、b、c三种元素中,原子半径最大的是钠,离子半径最大的是F-,
故答案为:钠;F-;
(4)NaOH和氢氧化铝反应生成偏铝酸钠和水,离子反应为OH-+Al(OH)3=AlO2-+2H2O,故答案为:OH-+Al(OH)3=AlO2-+2H2O;
(5)A.位于阶梯虚线附近的元素,在金属与非金属的交界处,则元素既表现某些金属的性质,又表现某些非金属的性质,故A正确;
B.在过渡元素区寻找催化剂,不能在阶梯虚线附近寻找催化剂,故B错误;
C.F无正价,不存在最高价含氧酸,高氯酸的酸性最强,故C错误;
D.由同主族从上到下金属性增强,同周期从左向右金属性减弱可知表中Cs的金属性最强,故D正确;
故答案为:BC.
点评 本题考查原子结构与元素周期律,为高频考点,把握元素在周期表的位置、元素周期律为解答的关键,侧重分析与应用能力的考查,注意规律性知识的应用,题目难度不大.

| A. | 氨水具有挥发性 | B. | 1mol/L硝酸铵溶液pH约为5 (室温) | ||
| C. | 氨水能与硫酸发生化学反应 | D. | 氨水导电能力较弱 |
| A. | 甲烷和乙烷 | B. | 丙烷和丁烷 | C. | 乙烷和乙烯 | D. | 戊烷和己烷 |
| A. | 次氯酸消毒餐具 | B. | 氧化铝做耐火材料 | ||
| C. | 焦炭用于炼铁工业 | D. | K、Na合金作原子反应堆导热剂 |
| A. | 12与17 | B. | 1与16 | C. | 11与8 | D. | 6与8 |
| A. | 无水硫酸铜 | B. | 石灰石 | C. | 金属钠 | D. | 胆矾 |
| A. | 该酒在55℃的条件下酿造 | B. | 该酒的沸点为55℃ | ||
| C. | 100mL该酒中含乙醇55mL | D. | 100g该酒中含乙醇55g |
| A. | 纤维素属于二糖,能发生水解,但不能发生银镜反应 | |
| B. | 蛋白质水解的最终产物为多肽 | |
| C. | 相对分子质量为105000的聚丙烯其聚合度为2500 | |
| D. | 仅用新制的氢氧化铜试剂可以证明淀粉已部分水解 |
| A. | (NH4)2SO4 | B. | Cl2 | C. | NH3 | D. | CH3COOH |