题目内容
实验室用0.10mol/L的NaOH溶液滴定某一元弱酸HA的滴定曲线如图所示。图中横轴为滴入的NaOH溶液的体积V(mL),纵轴为溶液的pH。下列叙述不正确的是

A.此一元弱酸HA的电离平衡常数Ka≈1×10-6mol/L
B.此弱酸的起始浓度约为1×10-2mol/L
C.此实验最好选用酚酞试液(变色范围8.0~10.0)做指示剂
D.当混合液pH=7时,溶液中c(HA)>c(A—)
D
【解析】
试题分析:A、根据图像可知滴定前溶液中氢离子浓度是10—4mol/L,当滴入10ml氢氧化钠溶液时恰好反应。由于弱酸的电离程度近似为1%,则弱酸的起始浓度为10—2mol/L,因此电离平衡常数K= ,A正确;B、根据以上分析可知弱酸的起始浓度是1×10-2mol/L,B正确;C、终点时生成的盐水解溶液显碱性,则此实验最好选用酚酞试液(变色范围8.0~10.0)做指示剂,C正确;D、当混合液pH=7时,说明HA过量,则溶液中c(A—)>c(HA),D错误,答案选D。
,A正确;B、根据以上分析可知弱酸的起始浓度是1×10-2mol/L,B正确;C、终点时生成的盐水解溶液显碱性,则此实验最好选用酚酞试液(变色范围8.0~10.0)做指示剂,C正确;D、当混合液pH=7时,说明HA过量,则溶液中c(A—)>c(HA),D错误,答案选D。
考点:考查酸碱中和反应滴定曲线的有关判断与原因

练习册系列答案
 口算题卡北京妇女儿童出版社系列答案
口算题卡北京妇女儿童出版社系列答案
相关题目
在25 ℃时,密闭容器中X、Y、Z三种气体的初始浓度和平衡浓度如下表:
物质 | X | Y | Z |
初始浓度/(mol·L-1) | 0.1 | 0.2 | 0 |
平衡浓度/(mol·L-1) | 0.05 | 0.05 | 0.1 |
下列说法错误的
A.反应达到平衡时,X的转化率为50%
B.反应可表示为X+3Y 2Z,其平衡常数为1 600
2Z,其平衡常数为1 600
C.增大压强使平衡向生成Z的方向移动,平衡常数增大
D.改变温度可以改变此反应的平衡常数
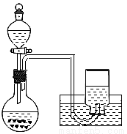
 ②乙同学认为“红色迅速褪去”是由于溶液中存在H2O2,其来源可能是Na2O2+2H2O=2NaOH+H2O2。简述你设计简单实验证明烧瓶内溶液中含H2O2的实验原理。
②乙同学认为“红色迅速褪去”是由于溶液中存在H2O2,其来源可能是Na2O2+2H2O=2NaOH+H2O2。简述你设计简单实验证明烧瓶内溶液中含H2O2的实验原理。
 ,有关说法正确的是
,有关说法正确的是
 (Ⅱ)已知某溶液中只存在OH-、H+、NH4+、Cl-四种离子,某同学推测该溶液中各离子浓度大小顺序可能有如下四种关系:
(Ⅱ)已知某溶液中只存在OH-、H+、NH4+、Cl-四种离子,某同学推测该溶液中各离子浓度大小顺序可能有如下四种关系: