题目内容
下列化学键中,一定属于极性共价键的是( )
| A、共价化合物中的化学键 |
| B、离子化合物中的共价键 |
| C、同种非金属元素原子间的共价键 |
| D、不同非金属元素原子间的共价键 |
考点:极性键和非极性键
专题:化学键与晶体结构
分析:同种非金属原子间形成非极性键,不同非金属原子间形成极性键,据此分析.
解答:
解:A、共价化合物中的化学键不一定是极性键,如C2H6中C-C键为非极性键,故A错误;
B、离子化合物中的共价键不一定是极性键,如Na2O2中的O-O键为非极性键,故B错误;
C、同种非金属元素原子间的共价键属于非极性键,故C错误;
D、不同非金属元素原子间的共价键属于极性键,故D正确;
故选D.
B、离子化合物中的共价键不一定是极性键,如Na2O2中的O-O键为非极性键,故B错误;
C、同种非金属元素原子间的共价键属于非极性键,故C错误;
D、不同非金属元素原子间的共价键属于极性键,故D正确;
故选D.
点评:本题考查了极性键和非极性键的判断,题目难度不大,注意把握极性键和非极性键的概念.

练习册系列答案
相关题目
相同体积的pH=3的强酸溶液和弱酸溶液分别跟足量的镁完全反应( )
| A、强酸溶液产生较多的氢气 |
| B、两者产生等量的氢气 |
| C、无法比较两者产生氢气的量 |
| D、弱酸溶液产生较多的氢气 |
下列离子或分子组成能大量共存,且满足相应要求的是( )


| A、A | B、B | C、C | D、D |
如图所示气体性质实验的常用装置,下列有关实验现象说法正确的是( )


| A、若水槽中是NaOH溶液,试管中是Cl2,可看到液面上升、试管中黄绿色褪去 |
| B、若水槽中是水,试管中是CO2,可看到液面上升并充满整个试管 |
| C、若水槽中是水并滴几滴酚酞,试管中是NH3,可看到液面上升并呈蓝色 |
| D、若水槽中是水并滴有几滴紫色石蕊,试管中是SO2,可看到液面上升并褪为无色 |
有机化合物A的分子式是C13H20O8(相对分子质量为304),1mol A在酸性条件下水解得到4mol CH3COOH和1mol B.B分子结构中每一个连有羟基的碳原子上还连有两个氢原子.B不能发生的反应是( )
| A、氧化反应 | B、取代反应 |
| C、消去反应 | D、加聚反应 |
下列物质的类别与所含官能团都正确的是( )
| A、酚类-OH |
| B、羧酸-CHO |
| C、醛类-COH |
| D、醚类 CH3-O-CH3 |
亮菌甲素适用于治疗急性胆囊炎,其结构简式如图.下列有关叙述正确的是( )
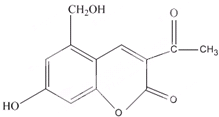

| A、亮菌甲素分子式为C12H11O5 |
| B、1mol亮菌甲素最多能与6mol H2发生加成反应 |
| C、1mol亮菌甲素与NaOH溶液反应,最多消耗3mol NaOH |
| D、亮菌甲素具有弱酸性体现了羟基对苯环的影响 |
在某100mL混酸中,硝酸的物质的量浓度为0.4mol?L-1,硫酸的物质的量浓度为0.2mol?L-1.向其中加入2.56g铜粉,微热,待充分反应后,溶液中Cu2+的物质的量浓度为( )
| A、0.15 mol?L-1 |
| B、0.3 mol?L-1 |
| C、0.225 mol?L-1 |
| D、无法计算 |
下列溶液中微粒的物质的量浓度关系一定正确的是( )
| A、pH=9的NaHA溶液:c(Na+)>c(HA-)>c(A2-)>c(H2A) |
| B、Na2CO3溶液:c(H+)-c(OH-)=c(HCO3-)+2c(CO32-)-c(Na+) |
| C、稀盐酸中加入一定量氨水后溶液显碱性:c(NH4+)>c(Cl-)>c(OH-)>c(H+) |
| D、将0.1mol?L-1 HF溶液与0.1mol?L-1 KF溶液等体积混合:c(F-)+c(HF)=0.2mol?L-1 |