题目内容
3.下列关于钠的说法中,不正确的是( )| A. | 金属钠和氧气反应,条件不同,产物则不同 | |
| B. | 钠原子的最外层只有一个电子 | |
| C. | 钠的化学性质很活泼,少量的钠可以保存在煤油中 | |
| D. | 当钠与硫酸铜溶液反应时,有大量红色固体铜出现 |
分析 A.常温下钠与氧气反应生成氧化钠,加热条件下与氧气反应可生成过氧化钠;
B.钠的原子序数为11,最外层只有1个电子;
C.钠性质活泼,常温下与氧气反应,钠可与水剧烈反应,实验室一般保存在煤油中;
D.钠性质活泼,与硫酸铜溶液反应时先和水反应生成氢氧化钠和氢气,最后生成氢氧化铜沉淀.
解答 解:A.常温下钠与氧气反应:4Na+O2=2Na2O,加热条件下与氧气反应2Na+O2$\frac{\underline{\;\;△\;\;}}{\;}$Na2O2,条件不同,产物则不同,故A正确;
B.钠元素的原子核内质子数是11,所原子结构示意图为 核外电子分三层排布,第一层2个第二层8个第三层1个,最外层只有一个电子,故B正确;
核外电子分三层排布,第一层2个第二层8个第三层1个,最外层只有一个电子,故B正确;
C.钠的密度比煤油大,且与煤油不反应,可保存在煤油中,故C正确;
D.钠性质活泼,与硫酸铜溶液反应时先和水反应2Na+2H2O=2NaOH+H2↑,生成氢氧化钠和铜离子反应生成氢氧化铜沉淀2OH-+Cu2+=Cu(OH)2↓,故D错误.
故选D.
点评 本题考查钠的结构和性质,题目难度不大,注意相关基础知识的积累,注意钠在常温下与在加热下与氧气反应的产物不同.

练习册系列答案
相关题目
11.(1)除去甲烷中的乙烯气体可用溴水(填试剂名称).实验方法为洗气(填操作名称).
(2)下列有关蒸馏乙醇和提纯苯甲酸实验的判断不正确的有b;
a.蒸馏乙醇的主要仪器有蒸馏烧瓶、温度计、冷凝管、铁架台、酒精灯、接液管和锥形瓶
b.如果温度计水银球位置低于支管口下沿,则收集的乙醇含有低沸点杂质
c.提纯苯甲酸时,用热水溶解,冷却后过滤除去固体杂质
d.测定苯甲酸晶体的熔点可能判断苯甲酸晶体是否为纯净物
(3)两种有机物A和B可以互溶,有关性质如下:
若要除去A和B的混合物中少量的B,可采用b(填代号)方法即可得到A.
a.重结晶 b.蒸馏 c.萃取 d.加水充分振荡,分液.
(2)下列有关蒸馏乙醇和提纯苯甲酸实验的判断不正确的有b;
a.蒸馏乙醇的主要仪器有蒸馏烧瓶、温度计、冷凝管、铁架台、酒精灯、接液管和锥形瓶
b.如果温度计水银球位置低于支管口下沿,则收集的乙醇含有低沸点杂质
c.提纯苯甲酸时,用热水溶解,冷却后过滤除去固体杂质
d.测定苯甲酸晶体的熔点可能判断苯甲酸晶体是否为纯净物
(3)两种有机物A和B可以互溶,有关性质如下:
| 相对密度(20℃) | 熔点 | 沸点 | 溶解性 | |
| A | 0.7893 | -117.3°C | 78.5°C | 与水以任意比混溶 |
| B | 0.7137 | -116.6°C | 34.5°C | 不溶于水 |
a.重结晶 b.蒸馏 c.萃取 d.加水充分振荡,分液.
8.某烃的结构简式为: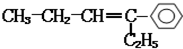 ,分子中含有四面体结构的碳原子(即饱和碳原子)数为a,在同一直线上的碳原子数量最多为b,在同一平面内的碳原子数最多为c,则a、b、c分别为( )
,分子中含有四面体结构的碳原子(即饱和碳原子)数为a,在同一直线上的碳原子数量最多为b,在同一平面内的碳原子数最多为c,则a、b、c分别为( )
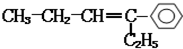 ,分子中含有四面体结构的碳原子(即饱和碳原子)数为a,在同一直线上的碳原子数量最多为b,在同一平面内的碳原子数最多为c,则a、b、c分别为( )
,分子中含有四面体结构的碳原子(即饱和碳原子)数为a,在同一直线上的碳原子数量最多为b,在同一平面内的碳原子数最多为c,则a、b、c分别为( )| A. | 4,3,10 | B. | 4,3,12 | C. | 4,2,7 | D. | 4,5,10 |
15.一种炔烃完全燃烧后,生成CO2和H2O的物质的量之比为5:4,则这种炔烃可能的结构有( )
| A. | 5种 | B. | 4种 | C. | 3种 | D. | 2种 |
12.某元素最高价氧化物对应水化物的分子式是H2RO4,则其氢化物的分子式是( )
| A. | RH4 | B. | RH3 | C. | H2R | D. | HR |
13.100mL6mol/LH2SO4跟过量的锌粉反应,在一定温度下,为了减缓反应速率,但又不影响生成氢气的总量.可向反应物中加入适量的( )
| A. | 碳酸钠(固体) | B. | 水 | C. | 硫酸钾溶液 | D. | 硫酸铵(固体) |
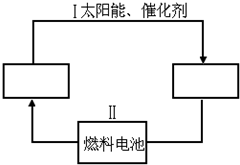 能源可化分为一级能源和二级能源.自然界以现成方式提供的能源称为一级能源;需依靠其他能源的能量间接制取的能源称为二级能源.氢气是一种高效而没有污染的二级能源,而如何快速制取出大量的氢气则成为发展氢能源的主要问题.
能源可化分为一级能源和二级能源.自然界以现成方式提供的能源称为一级能源;需依靠其他能源的能量间接制取的能源称为二级能源.氢气是一种高效而没有污染的二级能源,而如何快速制取出大量的氢气则成为发展氢能源的主要问题. .
.
 ;
;