题目内容
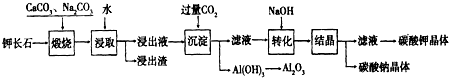
某科研小组以难溶性钾长石(K2O?Al2O3?6SiO2)为原料,提取Al2O3、K2CO3等物质,工艺流程如下:
(1)煅烧过程中有如下反应发生:
①钾长石中的硅元素在CaCO3作用下转化为CaSiO3,写出SiO2转化为CaSiO3的化学方程式: .
②钾长石中的钾元素和铝元素在Na2CO3作用下转化为可溶性的NaAlO2和KAlO2,写出Al2O3转化为NaAlO2的化学方程式: .
(2)已知NaAlO2和KAlO2易发生如下水解反应:AlO2-+2H2O?Al(OH)3+OH-.“浸取”时应保持溶液呈 性(填“酸”或“碱”),“浸取”时不断搅拌的目的是 .
(3)“转化”时加入NaOH的主要作用是(用离子方程式表示) .
(4)上述工艺中可以循环利用的主要物质是 、 和水.

(1)煅烧过程中有如下反应发生:
①钾长石中的硅元素在CaCO3作用下转化为CaSiO3,写出SiO2转化为CaSiO3的化学方程式:
②钾长石中的钾元素和铝元素在Na2CO3作用下转化为可溶性的NaAlO2和KAlO2,写出Al2O3转化为NaAlO2的化学方程式:
(2)已知NaAlO2和KAlO2易发生如下水解反应:AlO2-+2H2O?Al(OH)3+OH-.“浸取”时应保持溶液呈
(3)“转化”时加入NaOH的主要作用是(用离子方程式表示)
(4)上述工艺中可以循环利用的主要物质是
考点:物质分离和提纯的方法和基本操作综合应用
专题:实验设计题
分析:难溶性钾长石(K2O?Al2O3?6SiO2)为原料加入碳酸钙,碳酸钠高温煅烧后加入水浸取得到浸出渣为硅酸钙,浸取液位偏铝酸钠溶液,通入过量二氧化碳气体生成氢氧化铝沉淀过滤得到固体氢氧化铝.灼烧分解生成氧化铝;滤液中主要是碳酸氢钠溶液,加入氢氧化钠溶液反应生成碳酸钠,滤液主要是碳酸钾;
(1)①碳酸钙与二氧化硅在高温条件下反应生成硅酸钙和二氧化碳;
②氧化铝和碳酸钠在高温下反应生成偏铝酸钠和二氧化碳;
(2)偏铝酸根离子在碱性条件下不水解;浸取时不断搅拌目的是提高速率;
(3)碳酸氢根离子与氢氧根离子反应生成碳酸根离子和水;
(4)根据流程图推测可以循环利用的主要物质.
(1)①碳酸钙与二氧化硅在高温条件下反应生成硅酸钙和二氧化碳;
②氧化铝和碳酸钠在高温下反应生成偏铝酸钠和二氧化碳;
(2)偏铝酸根离子在碱性条件下不水解;浸取时不断搅拌目的是提高速率;
(3)碳酸氢根离子与氢氧根离子反应生成碳酸根离子和水;
(4)根据流程图推测可以循环利用的主要物质.
解答:
解:(1)①碳酸钙与二氧化硅在高温条件下反应生成硅酸钙和二氧化碳,该反应的化学方程式为:CaCO3+SiO2
CaSiO3+CO2↑,
故答案为:CaCO3+SiO2
CaSiO3+CO2↑;
②氧化铝和碳酸钠在高温下反应生成偏铝酸钠和二氧化碳,Al2O3+Na2CO3
2NaAlO2+CO2↑,故答案为:Al2O3+Na2CO3
2NaAlO2+CO2↑;
(2)偏铝酸根离子是强碱弱酸盐,在酸性溶液中会发生反应生成沉淀或铝离子,在中性溶液中会发生水解生成氢氧化铝,只有在碱性条件下,不反应不水解,所以在须在碱性条件下,“浸取”时不断搅拌能提高浸取速率,
故答案为:碱;提高浸取速率;
(3)碳酸氢根离子与氢氧根离子反应生成碳酸根离子和水,碳酸氢根离子是弱酸的酸根离子不能拆成碳酸根离子和氢离子,离子反应方程式为HCO3-+OH-=CO32-+H2O,故答案为:HCO3-+OH-=CO32-+H2O;
(4)煅烧时需要碳酸钠,在流程图提取碳酸钾之前可得到碳酸钠,所以碳酸钠为可循环利用的物质,在浸出液中需通二氧化碳,而碳酸钙与二氧化硅、氧化铝和碳酸钠在高温下反应都有二氧化碳生成,所以,二氧化碳是可循环使用的物质,
故答案为:Na2CO3;CO2.
| ||
故答案为:CaCO3+SiO2
| ||
②氧化铝和碳酸钠在高温下反应生成偏铝酸钠和二氧化碳,Al2O3+Na2CO3
| ||
| ||
(2)偏铝酸根离子是强碱弱酸盐,在酸性溶液中会发生反应生成沉淀或铝离子,在中性溶液中会发生水解生成氢氧化铝,只有在碱性条件下,不反应不水解,所以在须在碱性条件下,“浸取”时不断搅拌能提高浸取速率,
故答案为:碱;提高浸取速率;
(3)碳酸氢根离子与氢氧根离子反应生成碳酸根离子和水,碳酸氢根离子是弱酸的酸根离子不能拆成碳酸根离子和氢离子,离子反应方程式为HCO3-+OH-=CO32-+H2O,故答案为:HCO3-+OH-=CO32-+H2O;
(4)煅烧时需要碳酸钠,在流程图提取碳酸钾之前可得到碳酸钠,所以碳酸钠为可循环利用的物质,在浸出液中需通二氧化碳,而碳酸钙与二氧化硅、氧化铝和碳酸钠在高温下反应都有二氧化碳生成,所以,二氧化碳是可循环使用的物质,
故答案为:Na2CO3;CO2.
点评:本题主要考查了A1203、K2CO3等物质的提取,是工业流程题,依据相关的物质的性质,读懂流程是解答的关键,题目难度中等.

练习册系列答案
 智趣暑假温故知新系列答案
智趣暑假温故知新系列答案 英语小英雄天天默写系列答案
英语小英雄天天默写系列答案
相关题目
下列各种描述中,正确的是( )
| A、氯水具有杀菌消毒作用,其中起作用的物质是氯气 |
| B、加碘食盐中所加的“碘”一般是碘化钾 |
| C、区别氯化铁溶液和氢氧化铁胶体可以用丁达尔效应 |
| D、用干燥的有色布条可以检验氯化氢气体中是否混有氯气 |
下列物质都能有Na反应放出H2,其产生的H2的速率排列顺序正确的是( )
①C2H5OH;②CH3COOH;③NaCl(aq)
①C2H5OH;②CH3COOH;③NaCl(aq)
| A、①>②>③ |
| B、②>①>③ |
| C、③>①>② |
| D、②>③>① |
下列有关说法正确的是( )
| A、在同温同压下,相同体积的任何气体含有相同数目的原子 |
| B、氧化还原反应的判断依据是元素化合价是否有变化 |
| C、能导电的物质一定是电解质 |
| D、金属氧化物不一定是碱性氧化物 |