题目内容
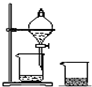
由短周期元素组成的中学常见物质A、B、C、D、E存在如图转化关系(部分生成物和反应条件略).
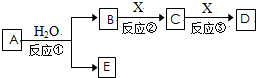
(1)若反应①在常温下进行,且E有漂白、杀菌作用,C是造成温室效应的主要气体,则:E的电离方程式为 ,反应③的离子反应方程式为 .
(2)若反应①是重要的工业反应之一,X是生产生活中使用最广泛的金属,则:
a.若B为气体单质,反应①的化学反应方程式为 .
b.若E为非金属氧化物,C的化学式为 .
(3)若A分子含有4个碳原子,D、E是同种有机物,75% B的水溶液常用于医疗消毒,则:反应①的化学反应方程式为 .
(4)若A由两种元素构成,B为气体,E为白色沉淀,B、E都能使酚酞试液变红,则反应①的化学反应方程式为 .

(1)若反应①在常温下进行,且E有漂白、杀菌作用,C是造成温室效应的主要气体,则:E的电离方程式为
(2)若反应①是重要的工业反应之一,X是生产生活中使用最广泛的金属,则:
a.若B为气体单质,反应①的化学反应方程式为
b.若E为非金属氧化物,C的化学式为
(3)若A分子含有4个碳原子,D、E是同种有机物,75% B的水溶液常用于医疗消毒,则:反应①的化学反应方程式为
(4)若A由两种元素构成,B为气体,E为白色沉淀,B、E都能使酚酞试液变红,则反应①的化学反应方程式为
考点:无机物的推断
专题:
分析:(1)反应①在常温下进行,且E有漂白、杀菌作用,C是造成温室效应的主要气体,则A为氯气,E为次氯酸,B为盐酸,C为二氧化碳X为碳酸盐;
(2)X是生产生活中使用最广泛的金属,X为Fe,B应为具有强氧化性的物质;
(3)75% B的水溶液常用于医疗消毒,则B为乙醇,A分子含有4个碳原子,D、E是同种有机物,则A为乙酸乙酯;
(4)B、E都能使酚酞试液变红,B、E为碱性物质,A由两种元素构成,与水反应生成B和E,B为气体,E为白色沉淀,则A氮化镁或氮化锂,B为氨气,E为氢氧化镁或氢氧化锂.
(2)X是生产生活中使用最广泛的金属,X为Fe,B应为具有强氧化性的物质;
(3)75% B的水溶液常用于医疗消毒,则B为乙醇,A分子含有4个碳原子,D、E是同种有机物,则A为乙酸乙酯;
(4)B、E都能使酚酞试液变红,B、E为碱性物质,A由两种元素构成,与水反应生成B和E,B为气体,E为白色沉淀,则A氮化镁或氮化锂,B为氨气,E为氢氧化镁或氢氧化锂.
解答:
解:(1)反应①在常温下进行,且E有漂白、杀菌作用,C是造成温室效应的主要气体,则A为氯气,E为次氯酸,B为盐酸,C为二氧化碳X为碳酸盐,E的电离方程式为HClO=H++ClO-,反应③的离子反应方程式为CO2+CO32-+H2O=HCO3-,故答案为:HClO=H++ClO-;CO2+CO32-+H2O=HCO3-;
(2)X是生产生活中使用最广泛的金属,X为Fe,B应为具有强氧化性的物质,
a、若B为气体单质,B为氯气,反应①为电解氯化钠溶液的反应,方程式为2Cl-+2H2O
2OH-+H2↑+Cl2↑,故答案为:2Cl-+2H2O
2OH-+H2↑+Cl2↑;
b、若E为非金属氧化物,E为NO,B为硝酸,C为硝酸铁[Fe(NO3)3],故答案为:Fe(NO3)3;
(3)75% B的水溶液常用于医疗消毒,则B为乙醇,A分子含有4个碳原子,D、E是同种有机物,则A为乙酸乙酯,反应①为乙酸乙酯在稀硫酸作用下水解反应,化学反应方程式为CH3COOC2H5+H2O
CH3COOH+C2H5OH,故答案为:CH3COOC2H5+H2O
CH3COOH+C2H5OH;
(4)B、E都能使酚酞试液变红,B、E为碱性物质,A由两种元素构成,与水反应生成B和E,B为气体,E为白色沉淀,则A氮化镁或氮化锂,B为氨气,E为氢氧化镁或氢氧化锂,反应①的化学反应方程式为Mg3N2+6H2O=3Mg(OH)2↓+2NH3↑或Li3N+3H2O=3LiOH↓+NH3↑,故答案为:Mg3N2+6H2O=3Mg(OH)2↓+2NH3↑或Li3N+3H2O=3LiOH↓+NH3↑.
(2)X是生产生活中使用最广泛的金属,X为Fe,B应为具有强氧化性的物质,
a、若B为气体单质,B为氯气,反应①为电解氯化钠溶液的反应,方程式为2Cl-+2H2O
| ||
| ||
b、若E为非金属氧化物,E为NO,B为硝酸,C为硝酸铁[Fe(NO3)3],故答案为:Fe(NO3)3;
(3)75% B的水溶液常用于医疗消毒,则B为乙醇,A分子含有4个碳原子,D、E是同种有机物,则A为乙酸乙酯,反应①为乙酸乙酯在稀硫酸作用下水解反应,化学反应方程式为CH3COOC2H5+H2O
| ||
| △ |
| ||
| △ |
(4)B、E都能使酚酞试液变红,B、E为碱性物质,A由两种元素构成,与水反应生成B和E,B为气体,E为白色沉淀,则A氮化镁或氮化锂,B为氨气,E为氢氧化镁或氢氧化锂,反应①的化学反应方程式为Mg3N2+6H2O=3Mg(OH)2↓+2NH3↑或Li3N+3H2O=3LiOH↓+NH3↑,故答案为:Mg3N2+6H2O=3Mg(OH)2↓+2NH3↑或Li3N+3H2O=3LiOH↓+NH3↑.
点评:本题考查无机物的推断,是高考中的常见题型,试题综合性强,难度较大,有利于培养学生的逻辑推理能力和抽象思维能力,提高学生分析问题、以及灵活运用基础知识解决实际问题的能力.做好本题的关键之处在于把握好常见物质的性质以及有关转化,并能结合题意具体问题、具体分析即可.

练习册系列答案
 优生乐园系列答案
优生乐园系列答案 新编小学单元自测题系列答案
新编小学单元自测题系列答案
相关题目
下列各组物质分类正确的一组是( )
| A、氧化物:水、双氧水、氧气 |
| B、碱:烧碱、纯碱、苛性钾 |
| C、盐:食盐、石灰石、生石灰 |
| D、酸:硫酸、醋酸、次氯酸 |
只用水不能鉴别的一组物质是( )
| A、乙醇和乙酸 | B、苯和乙醇 |
| C、苯和四氯化碳 | D、苯和溴苯 |
用惰性电极电解含有0.400molCu(NO3)2和0.400mol KCl的混合溶液,一段时间后,在一个电极上析出0.300mol Cu,此时在另一电极上放出的气体在标准状况下的体积(标准状况下)为( )
| A、3.36L |
| B、6.72L |
| C、5.60L |
| D、2.80L |
一定温度下,将3mol SO2和1mol O2充入一定容密闭容器中,在催化剂存在下进行下列反应:2SO2(g)+O2(g)?2SO3(g)△H=-197kJ/mol,当达到平衡状态时,下列说法中正确的是( )
| A、SO2与O2的转化率可能相等 |
| B、容器中一定存在n(SO2)>1mol且n(SO3)<2mol |
| C、放出的热量为197 kJ |
| D、当O2的转化率为50%时SO2和SO3的物质的量一定相等 |