题目内容
探究金属腐蚀:
[实验设计]
(1)实验用品:20% NaCl溶液、蒸馏水、酚酞溶液、KSCN溶液、新制氯水、纯铁丝、碳棒、U形管、导线等.
(2)实验方案:用导线连接铁丝和碳棒,并插入到盛有20% NaCl溶液的U形管中,放置数分钟.取插入铁丝的支管中的液体少许于一洁净试管中,滴入1~2滴KSCN溶液,未显红色,滴入氯水后显红色,证明有________生成,滴入氯水后显红色的离子方程式为________.在插入碳棒的支管中滴入酚酞溶液,碳棒周围溶液显红色,证明正极有________生成.
[拓展探究]
该研究性学习小组的同学又查阅了有关资料,得如下信息:
(1)O2在液滴表面和中心的浓度不同;(2)Fe2+在遇到K3[Fe(CN)6]时产生蓝色沉淀:3Fe2++2[Fe(CN)6]3-
答案:
解析:
解析:
|
答案: Fe2+ 2Fe2++Cl2 是 正极(液滴表面):2H2O+O2+4e- 讲析:钢铁在弱酸性或中性的环境中形成原电池而发生吸氧腐蚀,负极上 Fe失去电子生成Fe2+(Fe-2e- |

练习册系列答案
相关题目
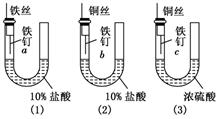
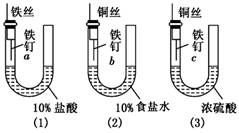
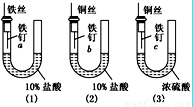
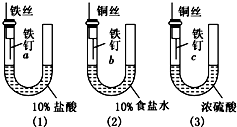 为了探究金属腐蚀的条件,某课外学习小组用不同的细金属丝将三根大小相同的普通铁钉分别固定在如下图所示的三个装置内,并将这些装置在相同的环境中放置相同的一段时间,下列对实验结果的描述不正确的是( )
为了探究金属腐蚀的条件,某课外学习小组用不同的细金属丝将三根大小相同的普通铁钉分别固定在如下图所示的三个装置内,并将这些装置在相同的环境中放置相同的一段时间,下列对实验结果的描述不正确的是( )| A、实验结束时,装置(1)左侧的液面一定会下降 | B、装置(2)中铁钉b发生电化学腐蚀 | C、实验结束时,装置(2)左边液面比右边高 | D、实验结束时,铁钉c腐蚀最严重 |