题目内容
13.工业上制取金刚砂的化学方程式如下:SiO2+3C=SiC+2CO↑.在这个氧化还原反应中,氧化剂和还原剂的物质的量之比为( )| A. | 1:2 | B. | 2:1 | C. | 5:3 | D. | 3:5 |
分析 该反应中C元素化合价由0价变为+2价和-4价,Si和O元素化合价不变,转移电子数为4,氧化剂和还原剂都是C,据此分析解答.
解答 解:反应SiO2+3C=SiC+2CO↑中,3个C中有1个C由0价降为-4价,得电子,作氧化剂,2个C由0价升为+2价,失电子,作还原剂,氧化剂和还原剂的物质的量之比为1:2,选A.
点评 本题考查氧化还原反应计算,为高频考点,侧重考查学生分析判断能力,明确化合价变化与氧化剂和还原剂关系是解本题关键,注意该反应中氧化剂和还原剂都是C,题目难度不大.

练习册系列答案
 科学实验活动册系列答案
科学实验活动册系列答案
相关题目
3.下列解释实验现象的反应方程式正确的是( )
| A. | 切开的金属Na暴露在空气中,光亮表面逐渐变暗2Na+O2═Na2O | |
| B. | 向AgCl悬浊液中滴加NaI溶液,白色沉淀变成黄色AgCl+I-═AgI+Cl- | |
| C. | Na2O2在潮湿的空气中放置一段时间,变成白色粘稠物2Na2O2+2CO2═2Na2CO3+O2 | |
| D. | 向NaHCO3溶液中加入过量的澄清石灰水,出现白色沉淀2HCO3-+Ca2++2OH-═CaCO3↓+CO32-+2H2O |
4.下列有关实验的说法正确的是( )
| A. | 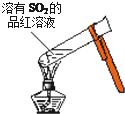 加热后溶液颜色变为无色 | B. |  配制100mL0.10mol•L-1NaCl溶液 | ||
| C. | 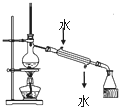 实验室用该装置制取少量蒸馏水 | D. |  称量25gNaOH |
1.提出元素周期律并根据周期律编制第一个元素周期表的科学家是( )
| A. | 道尔顿 | B. | 拉瓦锡 | C. | 门捷列夫 | D. | 阿伏加德罗 |
8.对于某些离子的检验及结论一定正确的是( )
| A. | 加入稀盐酸产生气体,将气体通入澄清石灰水,溶液变浑浊,一定有CO32- | |
| B. | 加入稀硝酸无明显现象,再加盐酸溶液产生沉淀,一定有Ag+ | |
| C. | 加入氯化钡溶液有白色沉淀产生,再加盐酸,沉淀不消失,一定有SO42- | |
| D. | 加入氯水,再加KSCN溶液显红色,一定有Fe3+ |
18.在一定温度下将amol PCl5充入一密闭容器中达到如下平衡:PCl5(g)?PCl3(g)+Cl2(g),此时压强为P1;再向容器中通入amol PCl5,在同温下又达到平衡时的压强为P2,则下列说法中正确的是( )
| A. | 2P1>P2 | B. | 2P1=P2 | C. | 2P1<P2 | D. | P1>P2 |
2.下列说法或表示法正确的是( )
| A. | 在101 kPa时,2 g H2完全燃烧生成液态水,放出285.8 kJ热量,氢气燃烧的热化学方程式表示为2H2+O2=2H2O△H=+285.8 kJ•mol-1 | |
| B. | 由C(石墨)→C(金刚石)△H=+119 kJ•mol-1可知,石墨不及金刚石稳定 | |
| C. | 在稀溶液中:H++OH-=H2O△H=-57.3 kJ•mol-1,若将含1mol CH3COOH的醋酸溶液与含1 mol NaOH的溶液混合,放出的热量大于57.3 kJ | |
| D. | CO(g)的燃烧热是283.0 kJ•mol-1,则2CO2(g)=2CO(g)+O2(g)反应的△H=+(2×283.0 )kJ•mol-1 |
3.往氯化铁溶液中分别加入下列类别的物质,不能产生Fe(OH)3的是( )
| A. | 单质 | B. | 氧化物 | C. | 碱 | D. | 酸 |
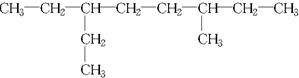
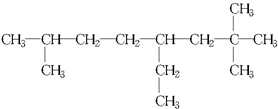
 .
. .
.