题目内容
写出下列反应的离子方程式:
(1)石灰石溶于稀盐酸 .
(2)氯气通入氢氧化钠溶液中 .
(3)稀硫酸与氢氧化钡溶液的反应 .
(4)向澄清石灰水中通入少量的二氧化碳 .
(1)石灰石溶于稀盐酸
(2)氯气通入氢氧化钠溶液中
(3)稀硫酸与氢氧化钡溶液的反应
(4)向澄清石灰水中通入少量的二氧化碳
考点:离子方程式的书写
专题:离子反应专题
分析:(1)反应生成氯化钙、水和二氧化碳;
(2)反应生成氯化钠、次氯酸钠和水;
(3)反应生成硫酸钡和水;
(4)反应生成碳酸钙和水.
(2)反应生成氯化钠、次氯酸钠和水;
(3)反应生成硫酸钡和水;
(4)反应生成碳酸钙和水.
解答:
解:(1)反应生成氯化钙、水和二氧化碳,离子反应为CaCO3+2H+=Ca2++CO2↑+H2O,故答案为:CaCO3+2H+=Ca2++CO2↑+H2O;
(2)反应生成氯化钠、次氯酸钠和水,离子反应为Cl2+2OH-=Cl-+ClO-+H2O,故答案为:Cl2+2OH-=Cl-+ClO-+H2O;
(3)反应生成硫酸钡和水,离子反应为Ba2++2OH-+2H++SO42-=BaSO4↓+2H2O,故答案为:Ba2++2OH-+2H++SO42-=BaSO4↓+2H2O;
(4)反应生成碳酸钙和水,离子反应为CO2+Ca2++2OH-=CaCO3↓+H2O,故答案为:CO2+Ca2++2OH-=CaCO3↓+H2O.
(2)反应生成氯化钠、次氯酸钠和水,离子反应为Cl2+2OH-=Cl-+ClO-+H2O,故答案为:Cl2+2OH-=Cl-+ClO-+H2O;
(3)反应生成硫酸钡和水,离子反应为Ba2++2OH-+2H++SO42-=BaSO4↓+2H2O,故答案为:Ba2++2OH-+2H++SO42-=BaSO4↓+2H2O;
(4)反应生成碳酸钙和水,离子反应为CO2+Ca2++2OH-=CaCO3↓+H2O,故答案为:CO2+Ca2++2OH-=CaCO3↓+H2O.
点评:本题考查离子反应方程式的书写,为高频考点,把握发生的反应及离子反应的书写方法为解答的关键,侧重复分解反应、氧化还原反应的离子反应考查,注意离子反应中保留化学式的物质,题目难度不大.

练习册系列答案
相关题目
在一定温度下在某体积不变的容器中发生可逆反应:X2(气)+Y2(气)═2XY(气),达到平衡状态的标志是( )
| A、容器内的总压强不随时间变化 |
| B、X2的物质的量浓度不随时间变化 |
| C、X2、Y2、XY 的物质的量浓度之比为1:1:2 |
| D、单位时间内生成nmolX2,同时生成nmolY2 |
下列叙述正确的是( )
| A、氯化钠溶液在电流作用下电离成钠离子和氯离子 |
| B、溶于水后能电离出氢离子的化合物一定是酸 |
| C、硫酸钡难溶于水,但硫酸钡属于电解质 |
| D、二氧化碳溶于水后所得物质能部分电离,故二氧化碳属于电解质 |
属于氧化还原反应的离子方程式的是( )
| A、CaCO3+2H+=Ca2++CO2↑+H2O |
| B、Fe(OH)3+3 H+═Fe3++3H2O |
| C、HCO3-+H+=CO2↑+H2O |
| D、2Na+2H2O=2Na++2OH-+H2↑ |
下列有关Fe(OH)3胶体的制备方法正确的是( )
| A、将1~2ml饱和FeCl3溶液逐滴滴到20ml 0.5 mol?L-1NaOH溶液中 |
| B、将1~2ml饱和FeCl3溶液逐滴加入到20ml沸水中,并继续加热至溶液呈红褐色后停止加热 |
| C、将1~2ml饱和FeCl3溶液逐滴加入到20ml冷水中,再加热至沸腾 |
| D、将1~2ml沸水加入到1~2ml FeCl3饱和溶液中,并用玻璃棒不断搅拌 |
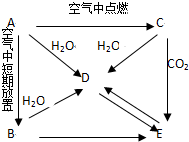 A、B、C、D、E五种物质都含同一种元素,C为一种淡黄色的固体.它们按如图所示的关系相互转化,已知A为单质.分别写出有关反应的化学方程式.
A、B、C、D、E五种物质都含同一种元素,C为一种淡黄色的固体.它们按如图所示的关系相互转化,已知A为单质.分别写出有关反应的化学方程式.