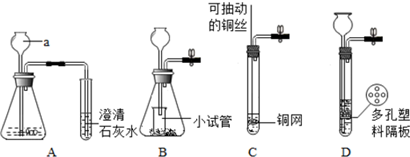
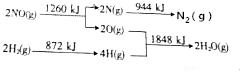
��Ŀ����
5���й�NaHCO3��Na2CO3�����ʣ���������������ǣ�������| A�� | ��������NaHCO3��Na2CO3���������ᷴӦ������ͬ������Na2CO3������CO2���С | |
| B�� | �����ʵ�������������ͬŨ��������ȫ��Ӧ����������������Na2CO3��NaHCO3������ | |
| C�� | ������NaHCO3��Na2CO3��������ȫ��Ӧ��ǰ����������϶� | |
| D�� | �����ʵ�����NaHCO3��Na2CO3���������ᷴӦ����CO2һ���� |
���� ��������NaHCO3��Na2CO3��Na2CO3�����ʵ�����С�������ʵ���ʱ�����ɶ�����̼��ͬ����Ϸ�Ӧ�Ļ�ѧ����ʽ�����⣮
��� �⣺A�����ݷ�Ӧ�ķ���ʽNa2CO3+2HCl=2NaCl+CO2��+H2O��NaHCO3+HCl=NaCl+CO2��+H2O��֪��106g̼������ȫ��Ӧ����1mol������̼��84g̼��������ȫ��Ӧ����1mol������̼����A��ȷ��
B���ɷ���ʽNa2CO3+2HCl=2NaCl+CO2��+H2O��NaHCO3+HCl=NaCl+CO2��+H2O��֪�������ʵ�������������ͬŨ��������ȫ��Ӧ����������������Na2CO3��NaHCO3����������B��ȷ��
C����������NaHCO3��Na2CO3��������ȫ��Ӧ��Na2CO3��������϶࣬��C����
D���ɷ���ʽNa2CO3+2HCl=2NaCl+CO2��+H2O��NaHCO3+HCl=NaCl+CO2��+H2O��֪�������ʵ�������������ͬŨ��������ȫ��Ӧ�����ɶ�����̼һ���࣬��D��ȷ��
��ѡC��
���� ���⿼����̼���ƺ�̼�����Ƶ����ʣ�Ϊ��Ƶ���㣬��Ŀ�ѶȲ�����ȷ���ʵ����ʡ������йػ�ѧ����ʽ�ļ����ǽ���ؼ���ע��̼���������ᷴӦ��ԭ����

��ϰ��ϵ�д�
�����Ŀ
16��ǿ���ǿ���ϡ��Һ��Ӧ���к��ȿ��Ա�ʾΪ��H+��aq��+OH-��aq��=H2O �� l ����H=-57.3kJ•mol-1��
��֪��CH3COOH ��aq��+NaOH ��aq��=CH3COONa ��aq��+H2O �� l ����H=-Q1 kJ•mol-1��
$\frac{1}{2}$H2SO4��Ũ��+NaOH ��aq��=$\frac{1}{2}$Na2SO4 ��aq��+H2O �� l ����H=-Q2 kJ•mol-1��
������Ӧ������Һ�н��У������й�ϵ��ȷ���ǣ�������
��֪��CH3COOH ��aq��+NaOH ��aq��=CH3COONa ��aq��+H2O �� l ����H=-Q1 kJ•mol-1��
$\frac{1}{2}$H2SO4��Ũ��+NaOH ��aq��=$\frac{1}{2}$Na2SO4 ��aq��+H2O �� l ����H=-Q2 kJ•mol-1��
������Ӧ������Һ�н��У������й�ϵ��ȷ���ǣ�������
| A�� | Q2��Q1��57.3 | B�� | Q1=57.3��Q2 | C�� | Q2��57.3��Q1 | D�� | Q2=57.3��Q1 |
20�����ҵĻ������÷����ܶ࣬���ú���Al2O3��SiO2������FeO•xFe2O3�������Ʊ�Al2��SO4��3•18H2O�������������£�
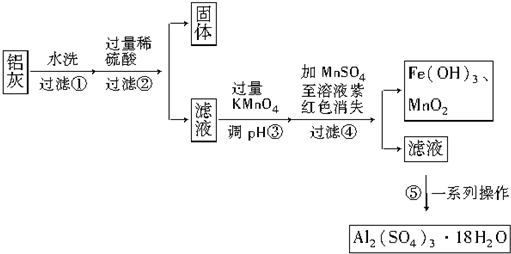
��ش��������⣺
��1���������ϡ�����ܽ�Al2O3�����ӷ���ʽ��6H++Al2O3�T2Al3++3H2O��
��2�������м����KMnO4Ҳ����H2O2���棬����H2O2������Ӧ�Ļ�ѧ����ʽΪH2O2+2FeSO4+H2SO4�TFe2��SO4��3+2H2O��
��3����֪��Ũ�Ⱦ�Ϊ0.1mol•L-1�Ľ��������ӣ������������������pH�����
����۵�Ŀ���ǽ�Fe2+����ΪFe3+����ʹFe3+ת��ΪFe��OH��3��������ȥ��
���ڸ�Ũ���³�ȥ���Ļ��������pH�����Χ��2.8��pH��3.4��
��4�������ܷ�����Ӧ�����ӷ���ʽΪ3Mn2++2MnO4-+2H2O�T5MnO2��+4H+��Ϊ����֤�ò������ù�����ȷʵ����MnO2����ѡ�õ��Լ���Ũ�����˫��ˮ��
��5�������ݡ�һϵ�в����������������в����õ���B������ţ���
A�������� B������ C�������� D���ƾ��� E��©����

��ش��������⣺
��1���������ϡ�����ܽ�Al2O3�����ӷ���ʽ��6H++Al2O3�T2Al3++3H2O��
��2�������м����KMnO4Ҳ����H2O2���棬����H2O2������Ӧ�Ļ�ѧ����ʽΪH2O2+2FeSO4+H2SO4�TFe2��SO4��3+2H2O��
��3����֪��Ũ�Ⱦ�Ϊ0.1mol•L-1�Ľ��������ӣ������������������pH�����
| Al��OH��3 | Fe��OH��2 | Fe��OH��3 | |
| ��ʼ����ʱ | 3.4 | 6.3 | 1.5 |
| ��ȫ����ʱ | 4.7 | 8.3 | 2.8 |
���ڸ�Ũ���³�ȥ���Ļ��������pH�����Χ��2.8��pH��3.4��
��4�������ܷ�����Ӧ�����ӷ���ʽΪ3Mn2++2MnO4-+2H2O�T5MnO2��+4H+��Ϊ����֤�ò������ù�����ȷʵ����MnO2����ѡ�õ��Լ���Ũ�����˫��ˮ��
��5�������ݡ�һϵ�в����������������в����õ���B������ţ���
A�������� B������ C�������� D���ƾ��� E��©����
10������˵����ȷ���ǣ�������
| A�� | ���Ӽ������������Ӽ���ڵľ������� | |
| B�� | ֻ�н����ͷǽ�������ʱ�����γ����Ӽ� | |
| C�� | �������Ӽ��Ļ�����һ�������ӻ����� | |
| D�� | �ڢ�A��͵ڢ�A��Ԫ��ԭ�ӻ���ʱ��һ���γ����ӻ����� |
17������˵����ȷ���ǣ�������
| A�� | ��ϩ������ϩ������ϩ����ʹ���Ը��������Һ��ɫ | |
| B�� | ����ʽΪC4H7ClO2������NaHCO3����CO2���л�����ܽṹ��3�� | |
| C�� | 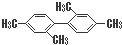 ������������11��̼ԭ�Ӵ���ͬһƽ���� ������������11��̼ԭ�Ӵ���ͬһƽ���� | |
| D�� | 1mol�л��� 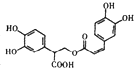 һ���������ܺ�7molNaOH��Ӧ һ���������ܺ�7molNaOH��Ӧ |
15��ij��ɫ������Һ�м��������ܷų�����������Һ��һ���ܴ���������������ǣ�������
| A�� | H+��Cu2+��Cl-��SO42- | B�� | HCO3-��NO3-��SO42-��Na+ | ||
| C�� | Cl-��SO42-��K+��Na+ | D�� | Fe3+��SO42-��Cl-��Al[��OH��4]- |