题目内容
19. 卤族元素的单质和化合物很多,我们可以利用所学物质结构与性质的相关知识去认识和理解.
卤族元素的单质和化合物很多,我们可以利用所学物质结构与性质的相关知识去认识和理解.(1)已知高碘酸有两种形式,化学式分别为H5IO6(
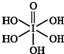 )和HIO4,前者为五元酸,后者为一元酸.请比较二者酸性强弱:H5IO6<HIO4(填“>”“<”或“=”).
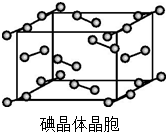
)和HIO4,前者为五元酸,后者为一元酸.请比较二者酸性强弱:H5IO6<HIO4(填“>”“<”或“=”).(2)图为碘晶体晶胞结构.有关说法中正确的是AD.
A.碘分子的排列有2种不同的取向,2种取向不同的碘分子以4配位数交替配位形成层结构
B.用均摊法可知平均每个晶胞中有4个碘原子
C.碘晶体为无限延伸的空间结构,是原子晶体
D.碘晶体中的碘原子间存在非极性键和范德华力.
分析 (1)根据含氧酸中,酸的元数取决于羟基氢的个数,含非羟基氧原子个数越多,酸性越强;
(2)同种非金属元素之间形成非极性共价键,碘为分子晶体,碘晶体中的碘原子间存在非极性键和范德华力,晶胞中占据顶点和面心,碘分子的排列有2种不同的取向.
解答 解:(1)H5IO6(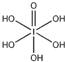 )中含有5个羟基氢,为五元酸,含非羟基氧原子1个,HIO4为一元酸,含有1个羟基氢,含非羟基氧原子3个,所以酸性:H5IO6<HIO4;
)中含有5个羟基氢,为五元酸,含非羟基氧原子1个,HIO4为一元酸,含有1个羟基氢,含非羟基氧原子3个,所以酸性:H5IO6<HIO4;
故答案为:<;
(2)A.碘分子的排列有2种不同的取向,在顶点和面心不同,2种取向不同的碘分子以4配位数交替配位形成层结构,故A正确;
B.用均摊法可知平均每个晶胞中有4个碘分子,即有8个碘原子,故B错误
C.碘晶体为无限延伸的空间结构,构成微粒为分子,是分子晶体,故C错误;
D.碘晶体中的碘原子间存在I-I非极性键,且晶体中分子之间存在范德华力,故D正确;
故答案为:AD.
点评 本题主要考查含氧酸酸性比较、晶体结构与性质,侧重物质结构与比较方法的考查,注意把握规律性知识的应用,题目难度中等.

练习册系列答案
 智慧小复习系列答案
智慧小复习系列答案
相关题目
19.设NA为阿伏加德罗常数的值,下列说法正确的是( )
| A. | 2.4g Mg在足量O2中燃烧,转移的电子数为0.1NA | |
| B. | 标准状况下,5.6L CO2气体中含有氧原子数为0.5NA | |
| C. | 氢原子数为0.4NA的CH3OH分子中含有的σ键数为0.4NA | |
| D. | 0.1L 0.5mol•L-1 CH3COOH溶液中含有的H+数为0.05NA |
20.设NA表示阿伏加德罗常数的值,下列叙述中正确的是( )
| A. | 常温常压下,22.4L O2所含的原子数为2NA | |
| B. | 标准状况下,22.4L H2所含的分子数为NA | |
| C. | 标准状况下,22.4L H2O所含的分子数为NA | |
| D. | 56g铁粉与盐酸完全反应时转移电子数为3NA |
14.下列物质中互为同分异构体的是②⑤,互为同素异形体的是③⑥,互为同位素的有④⑦,互为同系物的是⑨⑩,属于同一种物质的是①⑧.(填序号)
①液氯 ②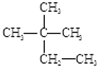 ③O2④18O ⑤
③O2④18O ⑤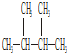
⑥O3⑦16O ⑧氯气 ⑨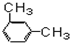 ⑩
⑩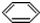
①液氯 ②
 ③O2④18O ⑤
③O2④18O ⑤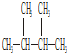
⑥O3⑦16O ⑧氯气 ⑨
 ⑩
⑩
4.下列叙述正确的是( )
| A. | H2O2的相对分子质量为34g | |
| B. | CH4的摩尔质量为16 g | |
| C. | 1 mol SO42--的质量为96g | |
| D. | 标准状况下1 mol H2O 的体积是22.4 L |
11.38.4g铜与过量稀硝酸充分反应,发生还原反应的HNO3的物质的量为( )
| A. | 1.2mol | B. | 1.6mol | C. | 0.4mol | D. | 0.2mol |
9.下列化学用语表达正确的是( )
| A. | 丙烷的球棍模型: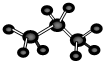 | B. | S2-的结构示意图: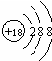 | ||
| C. | CO2的电子式:O=C=O | D. | 乙烯的结构简式:CH2CH2 |