题目内容
13.把1体积CH4和1体积Cl2组成的混合气体充入大试管中,将此试管倒立在盛有饱和食盐水的水槽里,放在光亮处.(1)试推测可观察到的现象:
①气体颜色变浅;②液面上升;③有油状液滴出现;④有白色晶体析出;
(2)若向饱和食盐水中加入紫色石蕊试液,又有什么现象?溶液变红;
(3)若将食盐水改为Na2SiO3溶液,则有什么现象产生?溶液中出现浑浊.
分析 (1)甲烷与氯气在光照条件下发生取代反应生成CH3Cl(气体)、CH2Cl2、CHCl3、CCl4、HCl,氯气逐渐减少甚至消失,氯气的颜色逐渐变浅或消失;反应后有油状液滴(二氯甲烷、三氯甲烷与四氯甲烷)出现;反应过程中气体的体积减小,导致试管内的压强低于外界大气压;氯化氢溶于水后溶液中氯离子浓度增大,导致氯化钠固体析出,溶液的pH变小;
(2)反应中有HCl生成,溶液呈酸性;
(3)反应后生成的氯化氢能够与硅酸反应生成硅酸沉淀.
解答 (1)甲烷与氯气在光照条件下发生取代反应生成CH3Cl(气体)、CH2Cl2、CHCl3、CCl4、HCl,随着氯气浓度的变小气体颜色变浅,反应生成的氯化氢极易溶于水,液面上升,反应后有油状液滴(二氯甲烷、三氯甲烷与四氯甲烷)出现;氯化氢溶于水后溶液中氯离子浓度增大,导致氯化钠固体析出,
故答案为:气体颜色变浅;液面上升;有油状液滴出现;有白色晶体析出;
(2)由于反应生成了氯化氢,所以反应后溶液为酸性,导致紫色石蕊试液变红,
故答案为:溶液变红;
(3)反应中有氯化氢生成,氯化氢与硅酸钠溶液反应生成硅酸,所以溶液中出现浑浊,
故答案为:溶液中出现浑浊.
点评 本题考查了甲烷的化学性质,题目难度不大,明确甲烷与氯气的反应实质为解答关键,注意该反应产物为CH3Cl(气体)、CH2Cl2、CHCl3、CCl4的混合物,试题培养了学生的化学实验能力.

练习册系列答案
 黄冈创优卷系列答案
黄冈创优卷系列答案
相关题目
4.设NA为阿伏加德罗常数的值.下列说法正确的是( )
| A. | 78g由Na2S和Na2O2组成的固体混合物,含有的阴离子数为NA | |
| B. | 标准状况下,22.4L CCl4中含有的分子数为NA | |
| C. | 将1mol FeCl3水解制成胶体,所得胶体中含有的胶体粒子数NA | |
| D. | 2.0gH218O与D2O的混合物中所含中子数为NA |
1.下列物质属于碱的是( )
| A. | Na2CO3 | B. | NaOH | C. | HCl | D. | BaSO4 |
8.下列关于烃的说法中正确的是( )
| A. | 烃是指分子里含有碳、氢元素的化合物 | |
| B. | 烃是指分子里含有碳元素的化合物 | |
| C. | 烃是指燃烧后能生成CO2和H2O的化合物 | |
| D. | 烃是指仅由碳和氢两种元素组成的化合物 |
5.下列表示对应化学反应的离子方程式正确的是( )
| A. | 向苯酚钠溶液中通入少量CO2:2C6H5O-+CO2+H2O→2C6H5OH+CO32- | |
| B. | 用石墨作电极电解氯化镁溶液:2Cl-+2H2O$\frac{\underline{\;通电\;}}{\;}$2OH-+H2↑+Cl2↑ | |
| C. | 向NH4HCO3溶液中滴加过量Ba(OH)2溶液:HCO3-+OH-+Ba2+═H2O+BaCO3↓ | |
| D. | NaAlO2溶液中通入过量二氧化碳:AlO2-+CO2+2H2O═Al(OH)3↓+HCO3- |
2.下列反应属于氧化还原反应的是( )
| A. | CaCO3═CaO+CO2↑ | B. | Na2CO3+2HCl═2NaCl+CO2↑+H2O | ||
| C. | 2Fe3++Cu═2Fe2++Cu2+ | D. | BaCl2+H2SO4═BaSO4↓+2HCl |
3.下列实验操作或装置(略去部分加持仪器)正确的是( )
| A. | 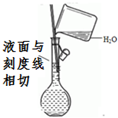 配制溶液 | B. | 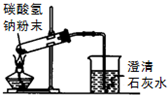 碳酸氢钠受热分解 | ||
| C. | 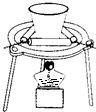 钠的燃烧 | D. | 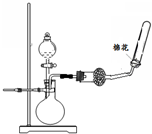 制取收集干燥的氨气 |
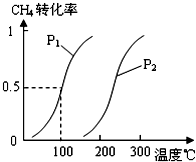 甲醇被称为2l世纪的新型燃料,工业上通过下列反应①②,用CH4和H2O为原料来制备甲醇.
甲醇被称为2l世纪的新型燃料,工业上通过下列反应①②,用CH4和H2O为原料来制备甲醇.