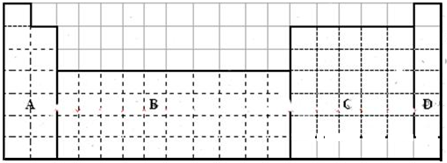
题目内容
3.A、B、C、D、E五种短周期元素,它们的原子序数依次增大;A是周期表中原子半径最小的元素;B的最高价氧化物的水化物与其氢化物能相互反应生成盐;A与C可形成两种液态化合物,其分子中电子总数分别为10和18;D元素的主族序数等于其周期数;E原子的最外层电子数是其电子层数的2倍.(1)E元素在周期表中的位置是第三周期第VIA族.
(2)五种元素原子半径从小到大的顺序为Al>S>N>O>H.
(3)A与C形成的18电子物质中所含的化学键类型是BC.
A.离子键 B.极性共价键 C.非极性共价键
(4)用电子式表示A和E形成的化合物的形成过程
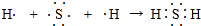 .
.(5)C和E的氢化物沸点较高的为H2O.
(6)写出B的最高价氧化物的水化物与其氢化物相互反应的化学方程式NH3+HNO3=NH4NO3.
分析 A、B、C、D、E五种短周期元素,它们的原子序数依次增大;A是周期表中原子半径最小的元素,则A为H元素;B的最高价氧化物的水化物与其氢化物能相互反应生成盐,则B为N元素;A与C可形成两种液态化合物,其分子中电子总数分别为10和18,则形成的化合物为H2O和H2O2,则C为O元素;D元素的主族序数等于其周期数,原子序数大于氧,则D为Al元素;由原子序数可知E处于第三周期,E元素原子的最外层电子数是其电子层数的2倍,则E为S元素.
解答 解:A、B、C、D、E五种短周期元素,它们的原子序数依次增大;A是周期表中原子半径最小的元素,则A为H元素;B的最高价氧化物的水化物与其氢化物能相互反应生成盐,则B为N元素;A与C可形成两种液态化合物,其分子中电子总数分别为10和18,则形成的化合物为H2O和H2O2,则C为O元素;D元素的主族序数等于其周期数,原子序数大于氧,则D为Al元素;由原子序数可知E处于第三周期,E元素原子的最外层电子数是其电子层数的2倍,则E为S元素.
(1)E为S元素,原子序数为16,核外有3个电子层,最外层电子数为6,位于周期表第三周期第VIA族,
故答案为:第三周期第VIA族;
(2)所有元素中H原子半径最小,同周期自左而右原子半径减小,一般电子层越多原子半径越大,故原子半径:Al>S>N>O>H,
故答案为:Al>S>N>O>H;
(3)A与C形成的18电子物质为H2O2,含H-O极性共价键、O-O非极性共价键,
故选:BC;
(4)A和E形成的化合物为H2S,用电子式表示其形成过程为: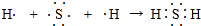 ,
,
故答案为: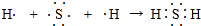 ;
;
(5)C、E的氢化物分别为H2O、H2S,水分子之间形成氢键,而硫化氢分子之间不能,故水的沸点高于硫化氢的,
故答案为:H2O;
(6)氮元素的最高价氧化物的水化物与其氢化物相互反应的化学方程式:NH3+HNO3=NH4NO3,
故答案为:NH3+HNO3=NH4NO3.
点评 本题考查位置、结构、性质的关系及应用,推断元素为解答的关键,注意氢键对物质性质的影响,掌握用电子式表示物质或化学键的形成.

| A. | 用氯化铁溶液鉴别苯酚溶液、辛烯、溴苯和乙醇四种有机物 | |
| B. | 用溴水鉴别苯、辛烯、甲苯和乙醇四种有机物 | |
| C. | 用酸性高锰酸钾溶液鉴别苯、甲苯、硝基苯四种液态有机物 | |
| D. | 用硫酸铜溶液除去乙炔中的杂质 |
| 0.01mol•L-1的溶液 | X | Y | Z | W |
| pH | 12 | 2 | 8.5 | 4.5 |
(2)HNO2在溶液中的电离方程式为HNO2?H++NO2-
(3)25℃时,W溶液的pH<7的原因是NH4++H2O?NH3•H2O+H+(用离子方程式表示).
(4)将X、Y、Z各1mol同时溶于水中制得混合溶液,则混合溶液中各离子的浓度由大到小的顺序为c(Na+)>c(NO3-)>c(NO2-)>c(OH-)>c(H+).
I:实验需要90mL 0.1mol/LFeBr2溶液
(1)配制FeBr2溶液除烧杯、玻璃棒、量筒、外还需的玻璃仪器是胶头滴管、100ml的容量瓶.
(2)下列有关配制过程中说法正确的是aef(填序号).
a.洗涤溶解FeBr2的烧杯和玻璃棒,并将洗涤液转移至容量瓶中
b.将称量的FeBr2放入容量瓶中,加90mL蒸馏水溶解
c.用托盘天平称量质量为1.9g的FeBr2
d.容量瓶贴签存放配好的FeBr2溶液
e.定容时,仰视容量瓶刻度线会使配制的FeBr2溶液浓度偏低
f.容量瓶查漏后没有干燥就进行配制,结果无影响
II:探究FeBr2的还原性
取10mL上述FeBr2溶液,向其中滴加少量新制的氯水,振荡后溶液呈黄色.某同学对产生黄色的原因提出了假设:
假设1:Br-被Cl2氧化成Br2溶解在溶液中;
假设2:Fe2+被Cl2氧化成Fe3+.
(3)请你完成表,验证假设:
| 实验步骤、预期现象 | 结论 |
| ①向溶液中加入适量苯,振荡、静置后 现象:CCl4层呈橙红色. | 假设1正确 |
| ②向溶液中加入KSCN溶液溶液 现象:溶液变为红色. | 假设2正确 |
请用一个离子方程式来证明:2Fe2++Br2=2Fe3++2Br-;
(5)若在50mL上述FeBr2溶液中通入5×10-3molCl2,则反应的离子方程式为:2Fe2++2Br-+2Cl2=2Fe3++Br2+4Cl-.
| A. | Cl的最高氧化物对应的水化物酸性最强 | |
| B. | S元素的族序数等于周期数3倍 | |
| C. | C元素的最高正价与最低负价代数和为零 | |
| D. | N元素的气态氢化物和它的最高价氧化物对应水化物能起化合反应 |
| A. | 水银 | B. | 青铜 | C. | 碳素钢 | D. | 不锈钢 |
| 选项 | 现象或反应 | 原理解释 |
| A | KI淀粉溶液中滴入氯水变蓝,再通入SO2,蓝色褪去 | SO2具有漂白性 |
| B | 合成氨反应需在高温条件下进行 | 该反应为吸热反应 |
| C | 蒸馏时,温度计的球泡应靠近蒸馏烧瓶支管口处 | 此位置指示的是被蒸馏物质的沸点 |
| D | 2CO=2C+O2在任何条件下均不能自发进行 | 该反应△H>0,△S<0 |
| A. | A | B. | B | C. | C | D. | D |