题目内容
10.欲测定Mg(NO3)2•n H2O中结晶水的含量,下列方案中肯定不可行的是( )| A. | 称量样品→加热→用已知质量的无水氯化钙吸收水蒸气并称量 | |
| B. | 称量样品→加热→冷却→称量Mg(NO3)2 | |
| C. | 称量样品→加热→冷却→称量MgO | |
| D. | 称量样品→加NaOH溶液→过滤→加热→冷却→称量MgO |
分析 测定Mg(NO3)2•nH2O里结晶水的含量,实验步骤为:①研磨 ②称量空坩埚和装有试样的坩埚的质量 ③加热 ④冷却 ⑤称量 ⑥重复③至⑤的操作,直到连续两次称量的质量差不超过0.1g为止 ⑦根据实验数据计算硝酸镁结晶水的含量,注意硝酸镁受热分解产物为氧化镁,据此分析判断.
解答 解:Mg(NO3)2受热易分解,其分解反应为:2Mg(NO3)2$\frac{\underline{\;\;△\;\;}}{\;}$2MgO+4NO2↑+O2↑.
A.称量样品→加热→用已知质量的无水氯化钙吸收水蒸气并称量,根据水的质量以及结晶水合物的质量可以求解,故A正确;
B.因硝酸镁易分解,称量样品→加热无法恰好使结晶水合物恰好分解为硝酸镁,故B错误;
C.称量样品→加热→冷却→称量MgO,根据硝酸镁分解的方程式以及氧化镁的质量可测定Mg(NO3)2•nH2O的结晶水含量,故C正确;
D.称量样品→加NaOH将硝酸镁转化为氢氧化镁,→过滤→加热氢氧化镁分解生成氧化镁→冷却→称量MgO,根据铜原子守恒求解无水硝酸镁的质量,据此求解结晶水含量,故D正确.
故选B.
点评 本题考查了通过晶体受热失水得到产物分析判断结晶水含量,明确物质的性质是解题关键,并注意某些物质的特征反应,题目难度不大.

练习册系列答案
 活力课时同步练习册系列答案
活力课时同步练习册系列答案 学业测评一课一测系列答案
学业测评一课一测系列答案
相关题目
5.X、Y、Z、W、J是元素周期表前四周期中的四种常见元素,其相关信息如表:
(1)元素Y在元素周期表的位置第三周期第VIA族.
(2)元素Z的原子最外层共有17种不同运动状态的电子.
(3)W的基态原子核外电子排布式是1s22s22p63s23p63d104s1.
(4)下列表述中能证明元素Y与元素Z非金属性较强的是cdf.
a.常温下,Y的单质与Z的单质状态不同
b.等物质的量浓度的氢化物水溶液的酸性不同
c.Z的电负性大于Y
d.Z的氢化物比Y的氢化物稳定
e.在反应中,Y原子得电子数比Z原子得电子数多
f.Z元素最高价氧化物对应水化物的酸性比Y元素最高价氧化物对应水化物的酸性强
(5)J的气态氢化物中心原子的杂化方式是sp3,与该原子形成的单质分子互为等电子体的含X元素的分子式为CO.
| 元素 | 相关信息 |
| X | X的基态原子核外3个能级上有电子,且每个能级上的电子数相等 |
| Y | M层上有2对成对电子 |
| Z | Z和Y同周期,Z的电负性大于Y |
| W | W的一种核素的质量数为63,中子数为34 |
| J | J的气态氢化物与J的最高价氧化物对应的水化物可反应生成一种盐 |
(2)元素Z的原子最外层共有17种不同运动状态的电子.
(3)W的基态原子核外电子排布式是1s22s22p63s23p63d104s1.
(4)下列表述中能证明元素Y与元素Z非金属性较强的是cdf.
a.常温下,Y的单质与Z的单质状态不同
b.等物质的量浓度的氢化物水溶液的酸性不同
c.Z的电负性大于Y
d.Z的氢化物比Y的氢化物稳定
e.在反应中,Y原子得电子数比Z原子得电子数多
f.Z元素最高价氧化物对应水化物的酸性比Y元素最高价氧化物对应水化物的酸性强
(5)J的气态氢化物中心原子的杂化方式是sp3,与该原子形成的单质分子互为等电子体的含X元素的分子式为CO.
1.常温下,饱和NaClO溶液的pH约为11.某消毒液的主要成分为NaClO,洁厕灵主要成分为HCl.下列解释相关事实的离子方程式中不合理的是( )
| A. | 用NaOH溶液吸收Cl2制备消毒液:Cl2+2OH-→Cl-+ClO-+H2O | |
| B. | 该消毒液与洁厕灵混用会引起中毒:2H++Cl-+ClO-→Cl2↑+H2O | |
| C. | 常温下,该消毒液的pH≈12是因为:ClO-+H2O?HClO+OH- | |
| D. | 该消毒液加少量白醋可增强消毒能力:CH3COOH+ClO-→HClO+CH3COO- |
18.在含有2mol复盐NH4Al(SO4)2的溶液中加入Ba(OH)2溶液,若生成4mol沉淀,则加入的Ba(OH)2的物质的量可能为( )
| A. | 6mol | B. | 4.7mol | C. | 3mol | D. | 2.4mol |
5.能够产生如图实验现象的液体是( )
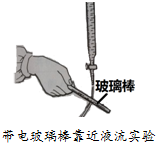

| A. | CS2 | B. | CCl4 | C. | H2O | D. |  |
15.新版人民币的发行,引发了人们对有关人民币中化学知识的关注.下列表述错误的是( )
| A. | 制造人民币所用的棉花、优质针叶木等原料含有C、H、O元素 | |
| B. | 用于人民币票面文字等处的油墨中所含有的Fe3O4是一种磁性物质 | |
| C. | 防伪荧光油墨由颜料与树脂等制成,其中树脂属于有机高分子材料 | |
| D. | 某种验钞笔中含有碘酒溶液,遇假钞呈现蓝色,其中遇碘变蓝的是葡萄糖 |
2.a L(标准状况)CO2通入100mL 3mol/L NaOH溶液的反应过程中所发生的离子方程式错误的是( )
| A. | a=3.36时,CO2+2OH-→CO32-+H2O | |
| B. | a=4.48时,2CO2+3OH-→CO32-+HCO3-+H2O | |
| C. | a=5.60时,3CO2+4OH-→CO32-+2HCO3-+H2O | |
| D. | a=6.72时,CO2+OH-→HCO3- |
19.Cl2可用于废水处理.向KCN溶液中先加入足量KOH溶液再通入氯气,充分反应后生成两种无毒的气体.下列说法正确的是( )
| A. | 两种无毒的气体均为还原产物 | |
| B. | 反应后溶液的pH会升高 | |
| C. | 氧化剂与还原剂的物质的量之比为5:2 | |
| D. | 每转移2NA个电子时,一定会生成13.44 L的气体 |
20.下列各组物质无论以何种比例混合,只要总的物质的量一定,完全燃烧时消耗氧气的量为定值的是( )
| A. | CH2O、C2H4O2、C6H12O6 | B. | C6H6O、C5H10、C7H6O2 | ||
| C. | C2H4,C2H5OH、HOCH2CH2COOH | D. | H2、CO、CH3OH |