题目内容
13.将4mol A和2mol B在2L的密闭容器中混合,并在一定条件下发生如下反应:2A(s)+B(g)?2C(g),反应2s后测得C的浓度为0.6mol/L.下列说法正确的是( )| A. | 用物质A表示2 s内的平均反应速率为0.3 mol/(L•s) | |
| B. | 用物质B表示2s内的平均反应速率为0.6 mol/(L•s) | |
| C. | 2 s后物质B的浓度为0.35 mol/L | |
| D. | 2 s后物质A的转化率为30% |
分析 反应2s后测得C的浓度为0.6mol/L,物质的量=0.6mol/L×2L=1.2mol,
2A(g)+B(g)?2C(g)
起始量(mol) 4 2 0
变化量(mol) 1.2 0.6 1.2
2s后(mol) 2.8 1.4 1.2
以此解答该题.
解答 解:反应2s后测得C的浓度为0.6mol/L,物质的量=0.6mol/L×2L=1.2mol,
2A(g)+B(g)?2C(g)
起始量(mol) 4 2 0
变化量(mol) 1.2 0.6 1.2
2s后(mol) 2.8 1.4 1.2
A.用物质A表示2 s内的平均反应速率为$\frac{\frac{1.2mol}{2L}}{2s}$=0.3 mol/(L•s),故A正确;
B.用物质B表示2s内的平均反应速率为$\frac{\frac{0.6mol}{2L}}{2s}$=0.15 mol/(L•s),故B错误;
C.2 s后物质B的浓度为$\frac{1.4mol}{2L}$=0.7 mol/L,故C错误;
D.2 s后物质A的转化率为$\frac{1.2}{4}×100%$=30%,故D正确.
故选AD.
点评 本题考查化学平衡计算,为高频考点,题目难度中等,涉及反应速率、平衡浓度、转化率的计算,明确反应速率与计量数的关系是解本题关键,会根据公式进行推导,试题培养了学生的化学计算能力.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
18.某实验小组利用如图装置(部分固定装置略)制备氮化钙(Ca3N2),并探究其实验式.
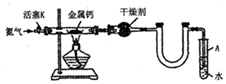
(1)按图连接好实验装置,检查装置的气密性,方法是关闭活塞K,微热反应管,试管A中有气泡冒出,停止加热.冷却后若末端导管中水柱上升且高度保持不变,则说明装置气密性良好.
(2)反应过程中末端导管必须始终插入试管A的水中,目的是防止反应过程中空气进入反应管.
(3)制备氮化钙的操作步骤是:①打开活塞K并通入N2;②点燃酒精灯,进行反应; ③反应结束后,防止反应过程中空气进入反应管;④拆除装置,取出产物.
(4)上述步骤①中通入N2-段时间后再点燃酒精灯原因是氮气排尽装置中的空气,可以防止钙与装置中的氧气或二氧化碳、水等反应,装置中干燥管后的U形管的作用是防倒吸.
(5)数据记录如表:
①计算得到实验式CaxN2,其中x=$\frac{14}{5}$.
②若通入的N2中混有少量O2,请比较x与3的大小,并给出判断依据:O2和N2分别与等量的Ca反应,生成CaO的质量高于Ca3N2.若通入的N2中混有少量的O2,会导致计算出n(N)偏大,所以 $\frac{n(Ca)}{n(N)}$<$\frac{3}{2}$,即x<3.

(1)按图连接好实验装置,检查装置的气密性,方法是关闭活塞K,微热反应管,试管A中有气泡冒出,停止加热.冷却后若末端导管中水柱上升且高度保持不变,则说明装置气密性良好.
(2)反应过程中末端导管必须始终插入试管A的水中,目的是防止反应过程中空气进入反应管.
(3)制备氮化钙的操作步骤是:①打开活塞K并通入N2;②点燃酒精灯,进行反应; ③反应结束后,防止反应过程中空气进入反应管;④拆除装置,取出产物.
(4)上述步骤①中通入N2-段时间后再点燃酒精灯原因是氮气排尽装置中的空气,可以防止钙与装置中的氧气或二氧化碳、水等反应,装置中干燥管后的U形管的作用是防倒吸.
(5)数据记录如表:
| 空瓷舟质量m0/g | 瓷舟与钙的质量m1/g | 瓷舟与产物的质量m2/g |
| 14.80 | 15.08 | 15.15 |
②若通入的N2中混有少量O2,请比较x与3的大小,并给出判断依据:O2和N2分别与等量的Ca反应,生成CaO的质量高于Ca3N2.若通入的N2中混有少量的O2,会导致计算出n(N)偏大,所以 $\frac{n(Ca)}{n(N)}$<$\frac{3}{2}$,即x<3.
5.下列反应属于氧化还原反应的是( )
| A. | CO+H2O$\frac{\underline{\;高温\;}}{\;}$H2+CO2 | B. | CaCO3+H2O+CO2═Ca(HCO3)2 | ||
| C. | CuO+2HCl═CuCl2+H2O | D. | CaCO3$\frac{\underline{\;\;△\;\;}}{\;}$CaO+CO2↑ |
2.某同学进行下列实验:下列说法合理的是( )
| 装置 | 操作 | 现象 |
 | 将盛有浓硝酸的烧杯A放入盛有淀粉KI溶液的烧杯C中,然后将铜片放入烧杯A后,立即用烧杯B罩住 | 烧杯A液体上方立即出现大量红棕色气体;一段时间后,红棕色气体消失,烧杯A和C中的液体都变成蓝色 |
| A. | 烧杯A中发生反应:3Cu+8HNO3═3Cu(NO3)2+2NO↑+4H2O | |
| B. | 红棕色气体消失只与NO2和烧杯C中的KI发生反应有关 | |
| C. | 烧杯C中溶液变蓝只与NO2和C中溶液发生反应有关 | |
| D. | 若将铜片换成铁片,则C中的液体也可能变蓝 |