题目内容
 合成氨是人类科学技术发展史上的一项重大突破,解决了地球上因粮食不足而导致的饥饿与死亡.
合成氨是人类科学技术发展史上的一项重大突破,解决了地球上因粮食不足而导致的饥饿与死亡.(1)氨分子的电子式为
(2)在一容积为2L的密闭容器内加入0.2mol的N2和0.6mol的H2,在一定条件下发生如下反应:N2(g)+3H2(g)?2NH3(g),反应中NH3的物质的量浓度的变化情况如图:
根据上图,计算从反应开始到平衡时,氢气的平均反应速率为
(3)催化剂存在下,NH3可用来消除NO的污染,生成两种对环境无害的物质.写出反应的化学方程式:
(4)pH相同的氨水和氢氧化钠溶液,分别用蒸馏水稀释至原来体积的m倍和n倍,稀释后两溶液的pH仍相同,则m
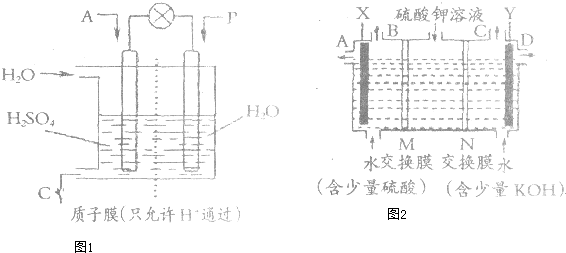
(5)氯碱工业的原料饱和食盐水中含有一定量的铵根离子,在电解时会生成性质极不稳定的三氯化氮,易引起爆炸.为除去饱和食盐水中的铵根离子,可在碱性条件下通入氯气,反应生成氮气.该反应的离子方程式为
考点:工业合成氨,反应速率的定量表示方法,化学平衡的影响因素
专题:氮族元素
分析:(1)氨气是氮原子和氢原子之间通过共价键形成的共价化合物;根据原子的最外层电子排布的轨道表示式的书写方法来回答;
(2)根据v(H2)=
c(NH3)进行计算;
(3)NH3可用来消除NO的污染,生成2种对环境无害的物质,应生成氮气和水;
(4)稀释后两种溶液的pH同,则溶液中c(OH-)相等,根据加水稀释时溶液中n(OH-)变化确定稀释后溶液体积的相对大小;
(5)可以根据反应物和生成物正确书写化学方程式,要充分理解化工生产中节能环保的意义.
(2)根据v(H2)=
| 3 |
| 2 |
(3)NH3可用来消除NO的污染,生成2种对环境无害的物质,应生成氮气和水;
(4)稀释后两种溶液的pH同,则溶液中c(OH-)相等,根据加水稀释时溶液中n(OH-)变化确定稀释后溶液体积的相对大小;
(5)可以根据反应物和生成物正确书写化学方程式,要充分理解化工生产中节能环保的意义.
解答:
解:(1)氨气是氮原子和氢原子之间通过共价键形成的共价化合物,电子式为: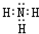 ,N原子的最外层电子排布的轨道表示式为:
,N原子的最外层电子排布的轨道表示式为: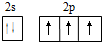 ,
,
故答案为: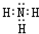 ;
; ;
;
(2)根据图象分析平衡时氨气的浓度为0.1mol/L,时间为4min,所以依据速率之比等于系数之比得到:v(H2)=
v(NH3)=
×
=0.0375 mol/(L?min),故答案为:0.0375 mol/(L?min);
(3)NH3可用来消除NO的污染,生成2种对环境无害的物质,应生成氮气和水,反应的方程式为4NH3+6NO
5N2+6H2O,反应中只有N元素化合价发生变化,由方程式可知反应中氧化产物与还原产物的物质的量之比为4:6=2:3,故答案为:4NH3+6NO
5N2+6H2O;2:3;
(4)一水合氨是弱电解质,氢氧化钠是强电解质,加水稀释过程中,促进氨水电离,导致氨水中n(OH-)增大,而氢氧化钠中n(OH-)不变,要使稀释后两种溶液的pH同,则溶液体积关系为:氨水>氢氧化钠,所以m>n,
故答案为:>;
(5)电解后的碱性溶液是氢氧化钠溶液,生成物是氮气、氯化钠、水.反应的离子方程式为:3Cl2+2NH4++8OH-═N2↑+6Cl-+8H2O;利用这种方法的优点很多,例如可以实现原料的再利用,环境污染程度降低等,利用废液作原料,变废为宝;或利用本厂生产的产品作原料,降低生产成本;或将NH4Cl杂质转化为N2,对环境无污染;
故答案为:3Cl2+2NH4++8OH-=N2↑+6Cl-+8H2O;就近取材,利用氯碱工业的产品氯气为原料(不会引入其他杂质离子).
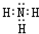 ,N原子的最外层电子排布的轨道表示式为:
,N原子的最外层电子排布的轨道表示式为: ,
,故答案为:
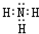 ;
; ;
;(2)根据图象分析平衡时氨气的浓度为0.1mol/L,时间为4min,所以依据速率之比等于系数之比得到:v(H2)=
| 3 |
| 2 |
| 3 |
| 2 |
| 0.1mol/L |
| 4min |
(3)NH3可用来消除NO的污染,生成2种对环境无害的物质,应生成氮气和水,反应的方程式为4NH3+6NO
| ||
| 高温高压 |
| ||
| 高温高压 |
(4)一水合氨是弱电解质,氢氧化钠是强电解质,加水稀释过程中,促进氨水电离,导致氨水中n(OH-)增大,而氢氧化钠中n(OH-)不变,要使稀释后两种溶液的pH同,则溶液体积关系为:氨水>氢氧化钠,所以m>n,
故答案为:>;
(5)电解后的碱性溶液是氢氧化钠溶液,生成物是氮气、氯化钠、水.反应的离子方程式为:3Cl2+2NH4++8OH-═N2↑+6Cl-+8H2O;利用这种方法的优点很多,例如可以实现原料的再利用,环境污染程度降低等,利用废液作原料,变废为宝;或利用本厂生产的产品作原料,降低生产成本;或将NH4Cl杂质转化为N2,对环境无污染;
故答案为:3Cl2+2NH4++8OH-=N2↑+6Cl-+8H2O;就近取材,利用氯碱工业的产品氯气为原料(不会引入其他杂质离子).
点评:本题考查了弱电解质的电离、化学方程式的书写及其化工生产中应该注意哪些问题,综合性强,难度不大.

练习册系列答案
相关题目
下列有机物命名实际上不可能存在的是( )
| A、2,2-二甲基丁烷 |
| B、3-甲基-2-丁烯 |
| C、4-甲基-1-戊炔 |
| D、1,3-二甲苯 |
用下列装置进行的实验中,能达到其实验目的是.( )
A、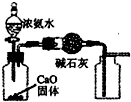 如图用装置制取并收集干燥纯净的NH3 |
B、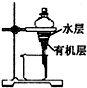 如图用装置分离苯萃取碘水后已分层的有机层和水层 |
C、 如图用装置配制一定的物质的量浓度的稀硫酸 |
D、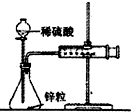 如图用装置测定锌与稀硫酸反应的速率 |
在FeCl3和CuCl2混合液中,加入一定量的铁粉,充分反应后,对溶液中阳离子(不考虑H+)的描述不正确的是( )
| A、容器底部没有固体,溶液中仅有Fe2+ |
| B、容器底部固体有铜和铁,溶液中只有Fe2+ |
| C、容器底部固体为铜,溶液中可能有Cu2+和Fe2+ |
| D、容器底部固体为铁粉,溶液中有Cu2+和Fe2+ |
下表数据是对应物质的熔点,下列说法正确的是( )
| 编号 | ① | ② | ③ | ④ |
| 物质 | AlF3 | AlCl3 | BCl3 | NCl3 |
| 熔点/℃ | 1291 | 160 | -107 | -40 |
| A、BCl3、NCl3分子中各原子最外层都满足8电子稳定结构 |
| B、因为键长B-F<B-Cl,故BF3的熔点高于BCl3 |
| C、AlF3、AlCl3都是强电解质,但晶体类型不同 |
| D、BCl3为平面正三角形分子,故它是由极性键构成的非极性分子 |