题目内容
煤矿瓦斯(含甲烷和氧气)爆炸是指,甲烷与氧气的比例在一定的范围内点火即爆炸.当甲烷与氧气的体积比为1:2时极易爆炸,此时甲烷与氧气的质量比是( )
| A、1:1 | B、1:2 |
| C、2:1 | D、1:4 |
考点:化学方程式的有关计算
专题:计算题
分析:同温同压下,甲烷与氧气的体积之比等于物质的量之比,再根据m=n×M计算质量之比,据此计算判断.
解答:
解:相同条件下,气体体积之比等于物质的量之比,相同条件下,甲烷和氧气的体积比为1:2时爆炸最为猛烈,则甲烷与氧气的物质的量之比为1:2,根据m=n×M,故此时甲烷与氧气的质量之比=1mol×16g/mol:2mol×32g/mol=1:4,
故选D.
故选D.
点评:本题考查阿伏伽德罗定律及推论的计算,题目难度不大,注意对公式的理解与灵活应用.

练习册系列答案
相关题目
某分子式为C10H20O2的酯,在一定条件下可发生如图的转化过程:则符合上述条件的酯的结构可有( )
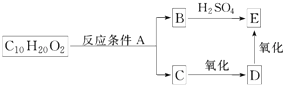

| A、2种 | B、4种 | C、6种 | D、8种 |
在标准状况下,将V L A气体(摩尔质量M g/mol)溶于100ml水中(A与水不反应),所得A的水溶液密度为ρ g/cm3,则此溶液的物质的量浓度(mol/L)为( )
A、
| ||
B、
| ||
C、
| ||
D、
|
酸雨形成的主要原因是( )
| A、森林乱伐,破坏生态平衡 |
| B、工业上大量含S燃料燃烧 |
| C、制H2SO4厂排出大量尾气 |
| D、汽车尾气的排放 |
向NaBr、NaI、Na2SO3混合液中,通入一定量氯气后,将溶液蒸干并充分灼烧,得到固体剩余物质的组成可能是( )
| A、NaBr Na2S04 |
| B、NaCl NaI Na2S04 |
| C、NaCl NaBr Na2S04 |
| D、NaCl Na2S03 |
某物质的结构简式为  ,其命名正确的是( )
,其命名正确的是( )
 ,其命名正确的是( )
,其命名正确的是( )| A、3-甲基-4-乙基-2-戊醇 |
| B、3,4-二甲基-5-己醇 |
| C、3,4-二甲基-2-己醇 |
| D、3-甲基-2-乙基-4-戊醇 |
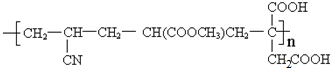
 用如图表示的一些物质或概念间的从属关系中不正确的是( )
用如图表示的一些物质或概念间的从属关系中不正确的是( )