题目内容
物质的量浓度为0.1mol/L的7种溶液:①HCl ②H2SO4③KCl ④Ba(OH)2⑤NaOH ⑥CH3COONa ⑦NH4NO3,其pH由小到大的顺序为 .
考点:pH的简单计算
专题:
分析:酸性:二元强酸>一元强酸>弱酸>强酸弱碱盐;碱性:二元强碱>一元强碱>强碱弱酸盐;溶液酸性越强,溶液的pH越小,溶液碱性越强,则溶液的pH越大,据此根据强弱电解质及盐的水解判断该溶液的pH大小.
解答:
解:①HCl是一元强酸,②硫酸为二元强酸,③氯化钾为强酸强碱盐,④Ba(OH)2是二元强碱,⑤氢氧化钠为一元强碱,⑥醋酸钠为强碱弱酸盐,⑦NH4NO3是强酸弱碱盐,
酸性,二元强酸>一元强酸>弱酸>强酸弱碱盐,则:②H2SO4>①HCl>⑦NH4NO3,
中性:③KCl,
碱性,二元强碱>一元强碱>强碱弱酸盐:④Ba(OH)2>⑤NaOH>⑥CH3COONa
溶液酸性越强,溶液的pH越小,溶液碱性越强,则溶液的pH越大,
所以这几种溶液pH由小到大的顺序为:②①⑦③⑥⑤④,
故答案为:②①⑦③⑥⑤④.
酸性,二元强酸>一元强酸>弱酸>强酸弱碱盐,则:②H2SO4>①HCl>⑦NH4NO3,
中性:③KCl,
碱性,二元强碱>一元强碱>强碱弱酸盐:④Ba(OH)2>⑤NaOH>⑥CH3COONa
溶液酸性越强,溶液的pH越小,溶液碱性越强,则溶液的pH越大,
所以这几种溶液pH由小到大的顺序为:②①⑦③⑥⑤④,
故答案为:②①⑦③⑥⑤④.
点评:本题考查了溶液酸碱性与溶液pH的关系,题目难度中等,注意掌握溶液酸碱性强弱的比较方法,明确溶液酸碱性与溶液pH的关系及盐的水解原理,试题培养了学生灵活应用所学知识解决实际问题的能力.

练习册系列答案
相关题目
某烃结构如图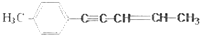 ,有关其结构说法正确的是( )
,有关其结构说法正确的是( )
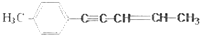 ,有关其结构说法正确的是( )
,有关其结构说法正确的是( )| A、所有原子可能在同一平面上 |
| B、在同一条直线上的碳原子最多有8个 |
| C、所有碳原子可能在同一平面上 |
| D、在同一平面上的原子最多有18个 |
室温,将一元酸HA的溶液和KOH溶液等体积混合(忽略体积变化),实验数据如表所示,下列说法不正确的是:( )
| 实验编号 | 起始浓度/mol/L | 反应后溶液pH | |
| c(HA) | c(KOH) | ||
| ① | 0.05 | 0.05 | 8 |
| ② | 0.1 | x | 7 |
| A、实验①中:C(K+)-C(A-)=9.9×10-7mol/L |
| B、实验②中C(K+)=C(A-)>C(H+)=C(OH-) |
| C、实验②中反应后溶液中C(K+)=0.05mol/L |
| D、若将实验②中HA换成氯水,反应后溶液pH=7,则有C(K+)=2C(ClO-)+C(HClO) |
相同温度相同物质的量浓度的三种溶液:①CH3COONa②NaHSO4③NaCl,按pH由大到小的顺序排列,正确的是( )
| A、③>②>① |
| B、①>③>② |
| C、①>②>③ |
| D、③>①>② |
下列反应中生成物总能量高于反应物总能量的是( )
| A、纯碱水解反应 |
| B、乙醇燃烧 |
| C、铝热反应 |
| D、氧化钙溶于水 |
在解释下列物质的性质变化规律与物质结构间的因果关系时,与键能无关的变化规律是( )
| A、与硅相比,金刚石的硬度大,熔点高 |
| B、HF、HCl、HBr、HI热稳定性依次减弱 |
| C、F2、Cl2、Br2、I2的沸点逐渐升高 |
| D、F2比O2更容易与H2反应 |
下列化学用语正确的是( )
| A、A乙醇的结构式:CH3CH2OH |
| B、乙烯的结构简式:C2H4 |
C、氯化钠的电子式: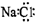 |
D、硫离子的结构示意图: |
用惰性电极电解MCl2的水溶液,当阴极上增重ag时,在阳极上同时产生bL气体(标准状况),则可知M的相对原子质量为( )
A、
| ||
B、
| ||
C、
| ||
D、
|