题目内容
下列各组离子中,可以在某种澄清透明溶液中大量共存的是( )
| A、ClO-、Na+、H+、Cl- |
| B、Mg2+、Cu2+、Cl-、SO42- |
| C、Na+、Ba2+、Cl-、CO32- |
| D、K+、H+、Fe2+、NO3- |
考点:离子共存问题
专题:离子反应专题
分析:如离子之间不发生复分解反应生成沉淀、气体、弱电解质,或不发生氧化还原反应、互促水解等反应,则可大量共存,否则不能,以此解答.
解答:
解:A.ClO-与H+反应生成弱酸HClO而不能大量共存,故A错误;
B.离子之间不发生任何反应,可大量共存,故B正确;
C.Ba2+与CO32-反应生成沉淀而不能大量共存,故C错误;
D.酸性条件下,Fe2+与NO3-发生氧化还原反应而不能大量共存,故D错误.
故选B.
B.离子之间不发生任何反应,可大量共存,故B正确;
C.Ba2+与CO32-反应生成沉淀而不能大量共存,故C错误;
D.酸性条件下,Fe2+与NO3-发生氧化还原反应而不能大量共存,故D错误.
故选B.
点评:本题考查离子共存问题,为高考常见题型,侧重于学生的分析能力和元素化合物知识的综合理解和运用的考查,注意把握常见离子的性质以及反应类型的判断,难度不大.

练习册系列答案
 浙大优学小学年级衔接导与练浙江大学出版社系列答案
浙大优学小学年级衔接导与练浙江大学出版社系列答案 小学暑假作业东南大学出版社系列答案
小学暑假作业东南大学出版社系列答案 津桥教育暑假拔高衔接广东人民出版社系列答案
津桥教育暑假拔高衔接广东人民出版社系列答案 波波熊暑假作业江西人民出版社系列答案
波波熊暑假作业江西人民出版社系列答案
相关题目
 X、Y、Z、W、R、E是六种短周期元素,如图是这六种元素的主要化合价与其原子序数的关系,下列说法不正确的是( )
X、Y、Z、W、R、E是六种短周期元素,如图是这六种元素的主要化合价与其原子序数的关系,下列说法不正确的是( )| A、原子半径:Z>W>R>E |
| B、R的气态氢化物比X的气态氢化物沸点高 |
| C、Z与Y可形成既含离子键又含共价键的化合物 |
| D、Z的最高价氧化物对应水化物与W的最高价氧化物对应水化物能发生反应 |
有一种锂电池,用金属锂和石墨作电极材料,电解质溶液是由四氯铝锂溶解在亚硫酰氯(SOCl2)中形成,电池的总反应式为8Li+3SOCl2═6LiCl+Li2SO3+2S,则下列叙述正确的是( )
| A、用该电池电解CuCl2溶液产生2.24L Cl2时,有0.2mol电子转移 |
| B、金属锂作电池的负极,石墨作电池的正极,加入硫酸可提高电解质的导电性 |
| C、电池工作(放电)过程中,SOCl2被还原为Li2SO3 |
| D、电池工作过程中,负极消耗的锂与正极生成的硫质量之比为7:8 |
在密闭容器中存在如下反应:A (g)+3B(g)?2C(g);△H<0,某研究小组研究了只改变某一条件对上述反应的影响,并根据实验数据作出下列关系图:

下列判断一定错误的是( )

下列判断一定错误的是( )
| A、图Ⅰ研究的是压强对反应的影响,且乙的压强较高 |
| B、图Ⅱ研究的是压强对反应的影响,且甲的压强较高 |
| C、图Ⅱ研究的是温度对反应的影响,且甲的温度较高 |
| D、图Ⅲ研究的是不同催化剂对反应的影响,且甲使用催化剂的效率较高 |
下列离子方程式书写不正确的是( )
| A、钠和冷水反应:Na+2H2O═Na++2OH-+H2↑ |
| B、铝粉投入到NaOH溶液中:2Al+2OH-+2H2O═2AlO2-+3H2↑ |
| C、AlCl3溶液中加入足量的氨水:Al3++4OH-═AlO2-+2H2O |
| D、FeCl2溶液跟Cl2反应:2Fe2++Cl2═2Fe3++2Cl- |
下列图示中关于实验操作或仪器的使用正确的是( )
A、 滴加液体 |
B、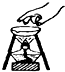 移走加热的蒸发皿 |
C、 液体药品的取用 |
D、 稀释浓硫酸 |