题目内容
8. 实验室需要450mL 1.0mol•L-1的硫酸溶液,某小组的同学设计如下实验步骤并依此进行配制,请回答相关问题.(已知所用98%浓硫酸的密度为1.84g/mL)
实验室需要450mL 1.0mol•L-1的硫酸溶液,某小组的同学设计如下实验步骤并依此进行配制,请回答相关问题.(已知所用98%浓硫酸的密度为1.84g/mL)①计算需98%的浓硫酸的体积;
②在烧杯中将浓硫酸稀释;
③接着将稀释后的硫酸转移到容量瓶中;
④洗涤烧杯和玻璃棒3次,并将洗涤液转移到容量瓶中;
⑤定容;
⑥摇匀.
(1)该实验中选用的定量仪器,除量筒外,还有500m容量瓶.
(2)该实验应该用(多大规格)50mL的量筒(可供选择的量筒规格为10mL、15mL、20mL、50mL和100mL),量取27.2 mL 98%的浓硫酸.
(3)①在配制过程中,如果没有洗涤烧杯和玻璃棒,其他操作都正确,那么所配溶液的实际浓度将偏小 (填“偏大、偏小、无影响”)
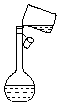
②某同学转移溶液的操作如图所示,该同学操作中的错误是未用玻璃棒引流.
③若用胶头滴管定容时,不小心滴水滴过了刻度线,你认为应该采取的处理方法是:重新配制.
④下列操作中,可能造成所配制溶液的浓度偏高的是abd(填选项).
a.溶解后没有冷却至室温就将液体转移至容量瓶中
b.定容时,俯视刻度线
c.洗涤后的容量瓶中残留少量蒸馏水
d.用量筒量取浓硫酸,读数时仰视刻度线.
分析 (1)依据配制一定物质的量浓度溶液的一般步骤选择仪器;依据配制溶液的体积选择合适规格的容量瓶;
(2)依据c=$\frac{1000ρω}{M}$计算浓硫酸的物质的量浓度,依据溶液稀释过程中溶质的物质的量不变计算需要浓硫酸的体积,依据浓硫酸体积选择量筒规格;
(3)①没有洗涤烧杯和玻璃棒导致溶质的物质的量偏小,依据c=$\frac{n}{V}$进行误差分析;
②移液时,应用玻璃棒引流;
③不当操作导致实验失败且无法补救的需要重新配制;
④分析不当操作对溶质的物质的量和溶液体积的影响,依据c=$\frac{n}{V}$进行误差分析.
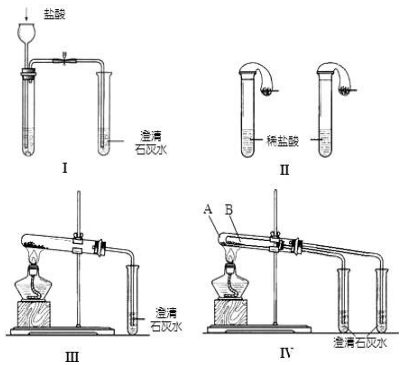
解答 解:(1)配制一定物质的量浓度溶液一般步骤为:计算、量取、稀释、移液、洗涤、定容等,用到的仪器有:量筒、烧杯、玻璃棒、容量瓶、胶头滴管,不需要的仪器有烧瓶和分液漏斗,要配制450mL溶液应选择500mL容量瓶,定量仪器:为量筒、500mL容量瓶;
故答案为:500mL容量瓶;
(2)98%浓硫酸的密度为1.84g/mL物质的量浓度为:$\frac{1000×1.84×98%}{98}$=18.4mol/L,设需要浓硫酸体积为V,则依据溶液稀释过程中溶质的物质的量不变得:18.4mol/L×V=500mL×1.0mol•L-1,解得V=27.2mL,应选择50mL量筒;
故答案为:50mL;27.2;
(3)①没有洗涤烧杯和玻璃棒导致溶质的物质的量偏小,依据c=$\frac{n}{V}$,导致溶液浓度偏低;
故答案为:偏低;
②该同学未用玻璃棒引流;
故答案为:未用玻璃棒引流;
③若用胶头滴管定容时,不小心滴水滴过了刻度线,导致实验失败且无法补救,需要:重新配制;
故答案为:重新配制;
④a.溶解后没有冷却至室温就将液体转移至容量瓶中,冷却后,溶液体积偏小,溶液浓度偏高,故a选;
b.定容时,俯视刻度线,导致溶液体积偏小,溶液浓度偏高,故b选;
c.洗涤后的容量瓶中残留少量蒸馏水,对溶质的物质的量和溶液体积都不产生影响,溶液浓度不变,故c不选;
d.用量筒量取浓硫酸,读数时仰视刻度线,导致量取浓硫酸体积偏大,硫酸的物质的量偏大,溶液浓度偏高,故d选;
故选:abd.
点评 本题考查一定物质的量浓度溶液的配制及误差分析,明确配制原理及操作步骤是解题关键,注意误差分析的方法和技巧.

| A. | 0.1 mol/L氨水中:c(NH4+)+c(H+)═c(OH-) | |
| B. | 0.1 mol/L的NH4Cl溶液中:c(NH4+)═c(Cl-) | |
| C. | 同为0.1 mol/L的硫酸和氨水等体积混合后:c(NH4+)+c(NH3•H2O)═2c(SO42-) | |
| D. | pH=3的盐酸和pH=11的氨水等体积混合后:c(OH-)=c(H+) |
| A. | HF+H2O?H3O++F- | |
| B. | NaHCO3=Na++HCO3-,HCO3-?H++CO32- | |
| C. | Ag2S(s)?2Ag+(aq)+S2-(aq) | |
| D. | S2-+2H2O?H2S+2OH- |
| A. | 相同温度下,1 mol•L-1氨水与0.5 mol•L-1氨水中c(OH-)之比是2:1 | |
| B. | 物质的量浓度相等的CH3COOH和CH3COONa溶液等体积混合:c(CH3COO-)+2c(OH-)═2c(H+)+c(CH3COOH) | |
| C. | 向0.2 mol•L-1 NaHCO3溶液中加入等体积0.1 mol•L-1 NaOH溶液:c(CO32-)>c(HCO3-)>c(OH-)>c(H+) | |
| D. | CH3COOH是弱电解质,NH3•H2O是弱电解质,故CH3COONH4也是弱电解质 |
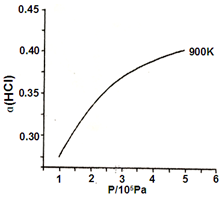 氯及其化合物在生活和生产中应用广泛.
氯及其化合物在生活和生产中应用广泛.