题目内容
12.下面对氯气的叙述正确的是( )| A. | 氯气可使湿的红布条褪色,所以氯气具有漂白性 | |
| B. | 氯气没有漂白性,但通入品红溶液中,品红褪色 | |
| C. | 氯气不跟非金属反应 | |
| D. | 氯气有毒,闻其气味时要小心将集气瓶放在鼻孔下直接闻其气味 |
分析 A、干燥的氯气不具有漂白性,潮湿的氯气具有漂白性,真正起作用的是次氯酸;
B、氯气与水反应生成的次氯酸具有漂白性;
C、在通常情况下,氯气能与氢气反应;
D、闻氯气时,不能直接放在鼻子下闻.
解答 解:A、因干燥的氯气不具有漂白性,氯气可使湿的红布条褪色,真正起作用的是氯气与水反应生成的次氯酸,故A错误;
B、因氯气与水反应生成的次氯酸,次氯酸具有漂白性,则通入品红溶液中可以使之褪色,故B正确;
C、在通常情况下,氯气能与氢气反应,故C错误;
D、闻氯气时,不能直接放在鼻子下闻,应用手在集气瓶口轻轻扇动来闻气体的气味,故D错误;
故选:B.
点评 本题主要考查氯气的化学性质,明确氯气与水、金属的反应以及次氯酸的性质是解答本题的关键.

练习册系列答案
 课时训练江苏人民出版社系列答案
课时训练江苏人民出版社系列答案
相关题目
3.如图表示在某溶液中滴加Ba(OH)2溶液时,生成的沉淀的物质的量随Ba(OH)2溶液的体积变化关系.该溶液的成分可能是 a( )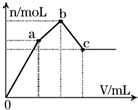

| A. | Na2SO4与NaAlO2组成的混合物 | B. | KAl(SO4)2 | ||
| C. | Al2(SO4)3 | D. | NH4Al(SO4)2 |
17.下列各组物质,前者逐滴滴加到后者中直至过量,先出现白色沉淀,后来沉淀又消失的是( )
| A. | H2SO4滴入NaAlO2溶液中 | B. | Ba(OH)2溶液滴入Al2(SO4)3溶液中 | ||
| C. | Al2(SO4)3溶液滴入NaOH溶液中 | D. | 氨水滴入Al2(SO4)3溶液中 |
4.一种新型燃料电池,它以多孔镍板为电极插入KOH溶液中,然后分别向两极上通乙烷和氧气,其电极反应式为:C2H6+18OH--14e-═2CO32-+12H2O,2H2O+O2+4e-═4OH-,有关此电池的推断正确的是( )
| A. | 电解质溶液中电子向正极移动 | |
| B. | 放电一段时间后,KOH的物质的量浓度不变 | |
| C. | 通乙烷的电极为负极 | |
| D. | 参加反应的O2和C2H6的物质的量之比为2:7 |
1.等体积的AlCl3和NaOH两种溶液混合后,沉淀物中含铝元素的质量与溶液中含铝元素的质量相等,则AlCl3和NaOH两种溶液物质的量浓度之比是( )
①1:3 ②1:4 ③2:3 ④2:7.
①1:3 ②1:4 ③2:3 ④2:7.
| A. | ③④ | B. | ①② | C. | ②④ | D. | ①③ |
2.短周期W、X、Y、Z四种元素的原子序数依次增大.W的某种原子无中子,X、Y形成的简单离子具有相同的电子层结构,且X、Y可形成原子个数比为1:1的具有漂白性的物质,工业上常用电解熔融的YZ来获得Y的单质.下列说法正确的是( )
| A. | 上述四种元素的原子半径大小顺序为r(Z)>r(Y)>r(X)>r(W) | |
| B. | W和X、Y、Z均能形成18电子的分子 | |
| C. | Y2X和Y2X2中阴、阳离子个数之比均为1:2 | |
| D. | X、Y、Z三种元素形成的化合物,其水溶液一定呈碱性 |
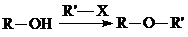 ②
②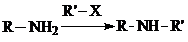
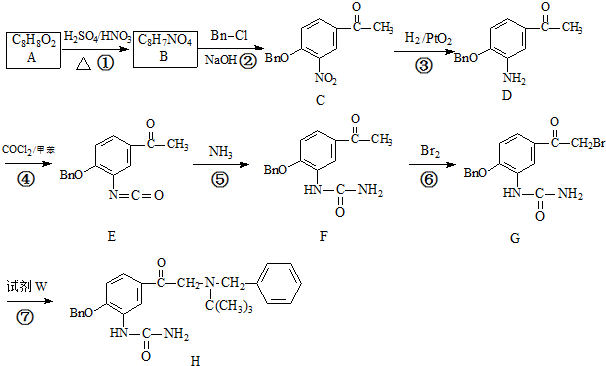
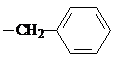 试剂W
试剂W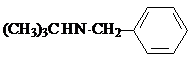 .
.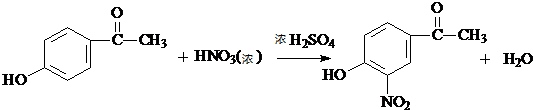 .
.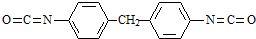 生成高聚物的结构简式
生成高聚物的结构简式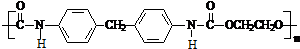 .
.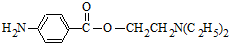 (无机试剂任用)(合成路线表示方式为:反应试剂A反应条件B…反应试剂反应条件目标产物)
(无机试剂任用)(合成路线表示方式为:反应试剂A反应条件B…反应试剂反应条件目标产物) 在一定条件下,N2和H2完全反应生成1molNH3放热46.0kJ热量.写出氨分解为氢气和氮气的热化学方程式2NH3(g)=N2(g)+3H2(g)△H=+92KJ/mol
在一定条件下,N2和H2完全反应生成1molNH3放热46.0kJ热量.写出氨分解为氢气和氮气的热化学方程式2NH3(g)=N2(g)+3H2(g)△H=+92KJ/mol
