题目内容
下列表达不正确的是( )
| A、反应2NO2═O2+2NO;△H=+116.2kJ/mol 任何情况非自发 |
| B、Na2CO3溶液中:c(Na+)=2c(CO32-)+2c(HCO3-)+2c(H2CO3) |
| C、表示碳燃烧热的热化学方程式为 C(s)+O2(g)=CO2(g);△H=-393.5kJ/mol |
| D、等物质的量的KHCO3和Ba(OH)2的溶液混合:HCO3-+Ba2++OH-=BaCO3↓+H2O |
考点:焓变和熵变,离子方程式的书写,热化学方程式,盐类水解的应用
专题:基本概念与基本理论
分析:A.△H-T△S<0的反应能够自发进行;
B.依据Na2CO3溶液中存在的物料守恒解答;
C.燃烧热是指1mol纯净物完全燃烧生成稳定的氧化物放出的热量,产物为稳定氧化物;
D.等物质的量的KHCO3和Ba(OH)2的溶液混合,反应生成碳酸钡沉淀和氢氧化钾、水.
B.依据Na2CO3溶液中存在的物料守恒解答;
C.燃烧热是指1mol纯净物完全燃烧生成稳定的氧化物放出的热量,产物为稳定氧化物;
D.等物质的量的KHCO3和Ba(OH)2的溶液混合,反应生成碳酸钡沉淀和氢氧化钾、水.
解答:
解:A.反应2NO2═O2+2NO;△H=+116.2kJ/mol,该反应气体体积增大,所以△S>O,而△H>0,当高温时,△H-T△S小于O,所以该反应在高温下能够自发进行,故A错误;
B.Na2CO3溶液中存在物料守恒,钠原子与碳原子个数比=2:1,存在c(Na+)=2c(CO32-)+2c(HCO3-)+2c(H2CO3),故B正确;
C.方程式中二氧化碳为气体,是最稳定的氧化物,且二氧化碳的物质的量为1mol,所以C(s)+O2(g)=CO2(g);△H=-393.5kJ/mol,是碳燃烧热的热化学方程式,故C正确;
D.等物质的量的KHCO3和Ba(OH)2的溶液混合,反应的离子方程式:HCO3-+Ba2++OH-=BaCO3↓+H2O,故D正确;
故选:A.
B.Na2CO3溶液中存在物料守恒,钠原子与碳原子个数比=2:1,存在c(Na+)=2c(CO32-)+2c(HCO3-)+2c(H2CO3),故B正确;
C.方程式中二氧化碳为气体,是最稳定的氧化物,且二氧化碳的物质的量为1mol,所以C(s)+O2(g)=CO2(g);△H=-393.5kJ/mol,是碳燃烧热的热化学方程式,故C正确;
D.等物质的量的KHCO3和Ba(OH)2的溶液混合,反应的离子方程式:HCO3-+Ba2++OH-=BaCO3↓+H2O,故D正确;
故选:A.
点评:本题为综合题,考查了反应自发进行的判断依据、物料守恒、燃烧热的定义、离子方程式的书写,题目难度不大,解题时应注意燃烧热的定义和物料守恒式子的书写.

练习册系列答案
相关题目
实验是研究化学的基础,下图中所示的实验方法、装置或操作完全正确的是( )
A、 除去氯气中的氯化氢 |
B、 称量 |
C、 用石灰石和稀盐酸制取CO2 |
D、 稀释 |
煤、石油、天然气是当今世界上最重要的化石燃料,下列关于它们的描述不正确的是( )
| A、燃烧时都会放出热量 |
| B、都是混合物 |
| C、都是重要的化工原料 |
| D、都是可再生能源 |
常温下,在10mL 0.2mol/L某一元强酸HA的溶液中逐滴加入a mL 0.1mol/L的氨水,下列有关说法中正确的是( )
| A、当c(NH4+)=c(A-)时,a一定等于20 |
| B、当c(NH4+)>c(A-)时,a一定大于20 |
| C、当c(H+)=c(OH-)时,a一定小于20 |
| D、当pH=7时,c(NH4+)=c(A-)=c(H+)=c(OH-) |
下列有关阿伏加德罗常数(NA)说法错误的是( )
| A、0.5 mol H2O含有的原子数目为1.5NA |
| B、标况下22.4L H2O所含的原子数目为3NA |
| C、1 mol H2O含有的H2O分子数目为NA |
| D、0.5NA个氯气分子的物质的量是0.5 mol |
下列化学实验基本操作中,正确的是( )
| A、稀释浓硫酸时,把浓硫酸慢慢倒入盛有水的量筒中并搅拌 |
| B、用量筒量取液体时,视线与量筒内液体保持水平 |
| C、用滴管滴加液体时,为防止液滴飞溅,滴管紧贴试管内壁 |
| D、用托盘天平称量物质时,称量物放在左盘,砝码放在右盘 |
下列说法不正确的是( )
| A、可通过酸性高锰酸钾溶液来区别烯烃和炔烃 |
| B、乙烯是石油裂解后的产物 |
| C、石油的分馏是物理变化,煤的干馏是化学变化 |
| D、现代工业生产中芳香烃主要来源于石油化工的催化重整和裂化 |
下列分散系不能发生丁达尔现象的是( )
| A、石灰水 | B、含有尘埃的空气 |
| C、雾 | D、彩色玻璃 |
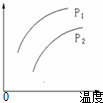 在容积一定的密闭容器中发生可逆反应A(g)+2B(g)?2C(g)-Q,条件变化时,影响平衡移动的关系如图所示.下列说法正确的是( )
在容积一定的密闭容器中发生可逆反应A(g)+2B(g)?2C(g)-Q,条件变化时,影响平衡移动的关系如图所示.下列说法正确的是( )| A、P1<P2,纵坐标指A的质量分数 |
| B、P1>P2,纵坐标指C的质量分数 |
| C、P1<P2,纵坐标指混合气体的平均摩尔质量 |
| D、P1>P2,纵坐标指A的转化率 |