题目内容
(1)化学反应可视为旧键断裂和新键形成的过程.化学键的键能是形成(或拆开)1mol化学键时释放(或吸收)的能量.已知:N≡N键的键能是948.9kJ?mol-1,H-H键的键能是436.0kJ?mol-1;由N2和H2合成1molNH3时可放出46.2kJ的热量.
N-H键的键能是 .
(2)根据下列热化学方程式分析,
C(S)+H2O(l)═CO(g)+H2(g);△H═+175.3KJ?mol-1
2CO(g)+O2(g)═2CO2(g);△H═-566.0KJ?mol-1
2H2(g)+O2(g)═2H2O(l);△H═-571.6KJ?mol-1
请写出表示C(S)的燃烧热的热化学反应方程式: .
N-H键的键能是
(2)根据下列热化学方程式分析,
C(S)+H2O(l)═CO(g)+H2(g);△H═+175.3KJ?mol-1
2CO(g)+O2(g)═2CO2(g);△H═-566.0KJ?mol-1
2H2(g)+O2(g)═2H2O(l);△H═-571.6KJ?mol-1
请写出表示C(S)的燃烧热的热化学反应方程式:
考点:有关反应热的计算,热化学方程式
专题:化学反应中的能量变化
分析:(1)根据断裂旧键要吸热,形成新键要放热,反应热等于反应物的总键能减去生成物的总键能计算;
(2)在25℃,101 kPa时,1 mol可燃物完全燃烧生成稳定的氧化物时所放出的热量,叫做该物质的燃烧热,表示C(S)的燃烧热的热化学反应方程式必须保证可燃物计量数为1,C元素转化为CO2,H元素转化为液态水,根据已知方程式和盖斯定律进行书写.
(2)在25℃,101 kPa时,1 mol可燃物完全燃烧生成稳定的氧化物时所放出的热量,叫做该物质的燃烧热,表示C(S)的燃烧热的热化学反应方程式必须保证可燃物计量数为1,C元素转化为CO2,H元素转化为液态水,根据已知方程式和盖斯定律进行书写.
解答:
解:(1)N2和H2合成NH3的方程式为:N2+3H2?2NH3,由N2和H2合成1molNH3时可放出46.2kJ/mol的热量,则反应的△H=-2×46.2=-92.4kJ/mol,
1molN2和3molH2反应断裂化学键需要吸收的能量为:1mol×948.9kJ?mol-1+3×436.0kJ?mol-1=2256.9kJ,
N-H键的键能为x,形成2molNH3需要形成6molN-H键,则形成6molN-H键放出的能量为6x,
则2256.9-6×x=-92.4kJ/mol,解得x=391.55kJ/mol,
故答案为:391.55kJ/mol;
(2)①C(S)+H2O(l)═CO(g)+H2(g)△H═+175.3KJ?mol-1
②2CO(g)+O2(g)═2CO2(g)△H═-566.0KJ?mol-1
③2H2(g)+O2(g)═2H2O(l)△H═-571.6KJ?mol-1
根据盖斯定律:由
得:C(s)+O2(g)═CO2(g)△H═-393.5 KJ?mol-1,
故答案为:C(s)+O2(g)═CO2(g)△H=-393.5 KJ?mol-1.
1molN2和3molH2反应断裂化学键需要吸收的能量为:1mol×948.9kJ?mol-1+3×436.0kJ?mol-1=2256.9kJ,
N-H键的键能为x,形成2molNH3需要形成6molN-H键,则形成6molN-H键放出的能量为6x,
则2256.9-6×x=-92.4kJ/mol,解得x=391.55kJ/mol,
故答案为:391.55kJ/mol;
(2)①C(S)+H2O(l)═CO(g)+H2(g)△H═+175.3KJ?mol-1
②2CO(g)+O2(g)═2CO2(g)△H═-566.0KJ?mol-1
③2H2(g)+O2(g)═2H2O(l)△H═-571.6KJ?mol-1
根据盖斯定律:由
| ①×2+②+③ |
| 2 |
故答案为:C(s)+O2(g)═CO2(g)△H=-393.5 KJ?mol-1.
点评:本题考查了键能与反应热的关系、C(S)的燃烧热的热化学反应方程式书写,题目难度中等,注意反应热等于反应物的总键能减去生成物的总键能,注意盖斯定律的应用.

练习册系列答案
相关题目
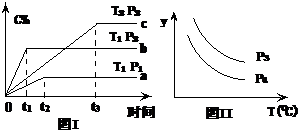 在某容积一定的密闭容器中,有下列的可逆反应:A(g)+B(g)?xC(g)(正反应放热)有图Ⅰ所示的反应曲线,
在某容积一定的密闭容器中,有下列的可逆反应:A(g)+B(g)?xC(g)(正反应放热)有图Ⅰ所示的反应曲线,试判断对图Ⅱ的说法中正确的是(T表示温度,P表示压强,C%表示C的体积分数)( )
| A、P3<P4 y轴表示A的转化率 |
| B、P3>P4 y轴表示B的百分含量 |
| C、P3>P4 y轴表示混合气体的密度 |
| D、P3>P4y轴表示混合气体的平均相对分子质量 |
构造原理揭示的电子排布能级顺序,实质是各能级能量高低.若以E(nl)表示某能级的能量,以下各式中正确的是( )
| A、E(4s)>E(3s)>E(2s)>E(1s) |
| B、E(3d)>E(4s)>E(3p)>E(3s) |
| C、E(5s)>E(4f)>E(4s)>E(3d) |
| D、E(5s)>E(4s)>E(4f)>E(3d) |
有a、b、c、d四种主族元素,已知a、b的阳离子和c、d的阴离子都具有相同的电子层结构,而且原子半径a>b,阴离子所带的负电荷数为c>d.则四种元素核电荷数由小到大的顺序为( )
| A、d<c<a<b |
| B、c<d<b<a |
| C、d<a<b<c |
| D、c<d<a<b |
用NA表示阿伏加德罗常数的值,下列叙述正确的是( )
| A、含有NA个氩原子的氩气在标准状况下的体积约为11.2 L |
| B、17g 氨气含有的电子数为10NA |
| C、18g D2O中含有的氧原子数为NA |
| D、标准状况下,22.4LCCl4含有的分子数为NA |
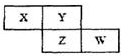 X、Y、Z、W四种短周期元素在周期表中的位置关系如图:若Z元素原子的最外层电子数是电子层数的2倍
X、Y、Z、W四种短周期元素在周期表中的位置关系如图:若Z元素原子的最外层电子数是电子层数的2倍