题目内容
5.某化学小组用大理石和稀盐酸反应制取二氧化碳气体,并进行性质实验.如图是有关实验的部分装置,请根据要求回答问题: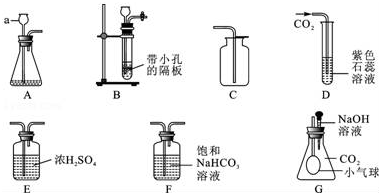
(1)a仪器的名称为长颈漏斗,甲同学用A和C组合制取二氧化碳,乙同学用B和C组合制取二氧化碳,你认为哪个同学的组合更便于控制反应乙(填“甲”或“乙”).
(2)甲同学利用装置D进行性质实验时,观察到紫色石蕊试液变红色,将红色液体充分加热未能重新变为紫色,你认为可能的原因是通入的二氧化碳气体中含有少量氯化氢气体;为使上述红色液体加热后能重新变为紫色,在气体通入装置D之前可接入上图装置F(填字母),在该装置中发生的主要化学反应方程式为NaHCO3+HCl=NaCl+H2O+CO2↑.
(3)乙同学将CO2通入到氢氧化钠溶液中,无明显现象,经过思考讨论后,设计了如图G装置,使该反应有了明显现象,则装置G中的现象为小气球逐渐膨胀起来.
分析 用大理石和稀盐酸反应制取二氧化碳气体,并进行性质实验,根据实验装置图可知,大理石为固体,盐酸为液体,反应不需要加热,为了便于控制反应可选用乙装置,因为氯化氢易挥发,所以制得的二氧化碳中含有氯化氢杂质,产生的二氧化碳要通过饱和碳酸氢钠溶液,可以除去气体中氯化氢,然后通过浓硫酸可得干燥的二氧化碳气体,可用向上排空气法收集二氧化碳气体,产生的二氧化碳气体可被氢氧化钠溶液吸收,使容器中的压强减小,所以检验二氧化碳与氢氧化钠的反应可用G装置进行,可观察到明显的现象,
(1)根据实验室常用仪器的名称和题中所指仪器的作用进行分析;
根据B装置可以利用气体的压强将固体和液体分离进行分析;
(2)根据盐酸具有挥发性进行分析;
根据碳酸氢钠和盐酸反应会生成二氧化碳气体进行分析;
(3)根据二氧化碳会与氢氧化钠反应,导致锥形瓶内的压强减小进行分析.
解答 解:用大理石和稀盐酸反应制取二氧化碳气体,并进行性质实验,根据实验装置图可知,大理石为固体,盐酸为液体,反应不需要加热,为了便于控制反应可选用乙装置,制得的二氧化碳中含有氯化氢杂质,所以产生的二氧化碳要通过饱和碳酸氢钠溶液,可以除去气体中氯化氢,然后通过浓硫酸可得干燥的二氧化碳气体,可用向上排空气法收集二氧化碳气体,产生的二氧化碳气体可被氢氧化钠溶液吸收,使容器中的压强减小,所以检验二氧化碳与氢氧化钠的反应可用G装置进行,可观察到明显的现象,
(1)仪器的图和用途可知a为长颈漏斗;在A装置中一旦石灰石和稀盐酸反应,则只有在至少一种反应物反应完全后,反应才能停止;而在B装置中,把石灰石放在隔板上,稀盐酸通过长颈漏斗加入,使用时,让稀盐酸与石灰石接触,反应开始,产生气体;不用时,可把导气管用止水夹夹住,产生的气体不能导出试管,造成试管内气体越来越多,压强越来越大,液体被压到长颈漏斗中,固体和液体分离,反应停止,所以乙同学的组合更便于控制反应,
故答案为:长颈漏斗;乙;
(2)盐酸具有挥发性,所以甲同学利用装置D进行性质实验时,观察到紫色石蕊试液变红色,将红色液体充分加热未能重新变为紫色,原因是:通入的二氧化碳气体中含有少量氯化氢气体,为使上述红色液体加热后能重新变为紫色,在气体通入装置D之前可接入如图装置F,碳酸氢钠和盐酸反应会生成二氧化碳气体、氯化钠和水,化学方程式为:NaHCO3+HCl=NaCl+H2O+CO2↑,
故答案为:通入的二氧化碳气体中含有少量氯化氢气体;F;NaHCO3+HCl=NaCl+H2O+CO2↑;
(3)二氧化碳会与氢氧化钠反应,导致锥形瓶内的压强减小,所以装置G中的现象为小气球逐渐膨胀起来.
故答案为:小气球逐渐膨胀起来.
点评 本题考查了实验室制取气体的发生装置、收集方法的选择以及气体的性质检验,可依据气体发生装置、收集方法的依据及气体的性质逐一分析.

 名校课堂系列答案
名校课堂系列答案| 编号 | 电极材料 | 电解质溶液 | 电流计指针偏转方向 |
| 1 | Mg、Al | 稀盐酸 | 偏向Al |
| 2 | Al、Cu | 稀盐酸 | 偏向Cu |
| 3 | Al、C(石墨) | 稀盐酸 | 偏向石墨 |
| 4 | Mg、Al | 氢氧化钠溶液 | 偏向Mg |
| 5 | Al、Zn | 浓硝酸 | 偏向Al |
(2)对实验3完成下列填空:铝为负极,电极反应2Al-6e-═2Al3+;石墨为正极,电极反应6H++6e-═3H2↑;
(3)实验4中铝作负极还是正极负极,铝电极的电极反应Al-3e-+4OH-═AlO2-+2H2O.

| A. | N2 | B. | H2S | C. | Mg | D. | Na |
| A. | 5种 | B. | 7种 | C. | 9种 | D. | 13种 |
| A. | 1s22s22p5 | B. | 1s22s22p43s2 | ||
| C. | 1s22s22p63s23p63d54s1 | D. | 1s22s22p63s23p63d34s2 |
| A. | 使用催化剂不改变反应速率 | B. | 降低压强能加快反应速率 | ||
| C. | 升高温度能加快反应速率 | D. | 改变压强对反应速率无影响 |
| A. | 粘有油脂的试管可以用热的纯碱溶液洗涤 | |
| B. | 食醋中含有乙酸,乙酸可由乙醇氧化得到 | |
| C. | 煤的气化、液化只发生物理变化 | |
| D. | 天然气作为化工原料主要用于合成氨和合成甲醇 |
| 选项 | 实验操作 | 实验目的 |
| A | 向盛有1mL2%的硝酸银溶液中逐滴加入2%稀氨水,边滴边振荡至最初产生的沉淀恰好消失为止 | 配制少量银氨溶液 |
| B | 向盛有2mL10%的硫酸铜溶液的试管中滴加0.5mL10%氢氧化钠溶液,混合均匀,滴入待检液,加热 | 检验某溶液中是否含有醛基 |
| C | 向淀粉溶液中加入稀硫酸,加热一段时间后,再加入银氨溶液 | 检验淀粉是否水解完全 |
| D | 将氯乙烷与氢氧化钠溶液共热一段时间,再向冷却后的混合溶液中滴加硝酸银溶液 | 检验水解产物中的氯离子 |
| A. | A | B. | B | C. | C | D. | D |