题目内容
20.选择适宜的材料和试剂设计一个原电池,以便完成下列反应.画出你的设计简图.Cu+2AgNO3═2Ag+Cu(NO3)2(1)请指出正极材料、负极材料、电解质溶液(写化学式)正极:Ag等,负极:Cu,电解质溶液:AgNO3.
(2)写出电极反应式:
正极:Ag++e-=Ag;负极:Cu-2e-=Cu2+.
(3)溶液中阳离子向正极移动,电子从负极流向正极.
分析 (1)根据“Cu+2AgNO3═2Ag+Cu(NO3)2”知,该反应中Cu元素化合价由0价变为+2价、Ag元素化合价由+1价变为0价,则Cu失电子发生氧化反应、银离子得电子发生还原反应,所以Cu作负极、不如Cu活泼的金属或导电的非金属作正极,硝酸银为电解质;
(2)正极上银离子得电子发生还原反应、负极上Cu失电子发生氧化反应;
(3)放电时,电解质溶液中阴离子向负极移动,阳离子向正极移动,电子从负极沿导线流向正极.
解答 解:(1)根据“Cu+2AgNO3═2Ag+Cu(NO3)2”知,在原电池中失电子的金属作负极,所以Cu作负极;不如Cu活泼的金属或导电的非金属作正极,如Ag等,硝酸银为电解质,
故答案为:Ag等;Cu;AgNO3;
(2)正极上银离子得电子发生还原反应、负极上Cu失电子发生氧化反应,正负极电极反应式分别为Ag++e-=Ag、Cu-2e-=Cu2+,
故答案为:Ag++e-=Ag;Cu-2e-=Cu2+;
(3)放电时,电解质溶液中阴离子向负极移动,阳离子向正极移动,负极上失电子、正极上得电子,所以电子从负极沿导线流向正极,
故答案为:正;负;正.
点评 本题考查原电池设计,为高频考点,明确正负极与反应类型的关系是解本题关键,难点是电解质溶液的确定,注意放电时电解质溶液中阴阳离子移动方向,为易错点.

练习册系列答案
相关题目
10.下列物质中存在顺反异构体的是( )
| A. | 2-氯丙烯 | B. | 1,2-二氯乙烯 | C. | 2-甲基-2-丁烯 | D. | 1-丁烯 |
8.下列离子方程式不正确的是( )
| A. | 乙酸与碳酸钠溶液反应:2CH3COOH+CO32-═2CH3COO-+CO2↑+H2O | |
| B. | 醋酸溶液与新制氢氧化铜反应:2CH3COOH+Cu(OH)2→Cu2++2CH3COO-+2H2O | |
| C. | 苯酚钠溶液中通入少量二氧化碳:2C6H5O-+CO2+H2O$\stackrel{△}{→}$2C6H5OH+CO | |
| D. | 甲醛溶液与足量的银氨溶液共热HCHO+4[Ag(NH3)2]++4OH-$\stackrel{△}{→}$CO32-+2NH4++4Ag↓+6NH3+2H2O |
5.下列反应中,最终一定有白色沉淀生成的是( )
①向久置的Na2SO3溶液中加入BaCl2溶液,再加入稀盐酸;②向Na2CO3溶液中加入酸化的CaCl2溶液;③向Na2SO3溶液中通入Cl2,再滴入BaCl2和稀盐酸;④向Na2SO3溶液中加入稀HNO3后再加入BaCl2溶液.
①向久置的Na2SO3溶液中加入BaCl2溶液,再加入稀盐酸;②向Na2CO3溶液中加入酸化的CaCl2溶液;③向Na2SO3溶液中通入Cl2,再滴入BaCl2和稀盐酸;④向Na2SO3溶液中加入稀HNO3后再加入BaCl2溶液.
| A. | ①④ | B. | ①②③④ | C. | ③④ | D. | ①③④ |
10.下列叙述中正确的是( )
| A. | 氯水、二氧化硫、活性炭的漂白或脱色原理虽然不同,但它们都能使品红或墨迹褪色 | |
| B. | 等物质的量的Cl2和SO2同时与潮湿的红布条作用,红布条立即褪色 | |
| C. | 反应CuSO4+H2S=CuS↓+H2SO4能进行,说明硫化铜既不溶于水,也不溶于稀硫酸 | |
| D. | 经Cl2和SO2漂白的物质,日后都会恢复原来的颜色 |
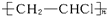 .
.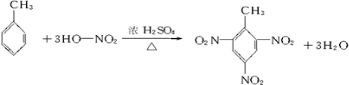 .
. (2)水
(2)水 (3)氮气
(3)氮气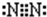 (4)氯化钠
(4)氯化钠
 (6)氢气H:H(7)氯化镁
(6)氢气H:H(7)氯化镁 (8)二氧化碳
(8)二氧化碳 .
.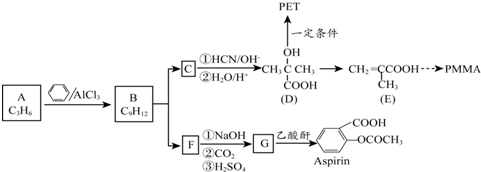
 .1mol Aspirin分子与足量的NaOH反应的化学方程式是
.1mol Aspirin分子与足量的NaOH反应的化学方程式是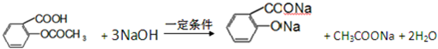 .
.