题目内容
工业废气中的氮氧化物是主要的大气污染物之一.为了治理污染,工业上常用氨气与之发生反应:NOx+NH3→N2+H2O,使其转化为无毒的N2.现有NO2和NO的混合气体3.0L,跟3.5L(同温同压下)NH3反应,恰好使其全部转化为氮气,则原混合气体中,NO2与NO的体积比是 .
考点:有关混合物反应的计算
专题:计算题
分析:先根据方程式3NOx+2xNH3=
N2+3xH2O计算x值,再利用十字相乘法计算二氧化氮和一氧化氮的体积比.
| 3+2x |
| 2 |
解答:
解:3NOx+2xNH3=
N2+3xH2O,
3 2x
3.0L 3.5L
则:x=
=1.75,
故氮氧化物的分子式为NO1.75,平均相对分子质量为42,则氮氧化物的平均化学式计算NO2与NO的体积比,
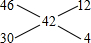 ,
,
所以二氧化氮和一氧化氮的体积比为:12:4=3:1,
故答案为:3:1.
| 3+2x |
| 2 |
3 2x
3.0L 3.5L
则:x=
| 3.5L×3 |
| 3.0×2 |
故氮氧化物的分子式为NO1.75,平均相对分子质量为42,则氮氧化物的平均化学式计算NO2与NO的体积比,
 ,
,所以二氧化氮和一氧化氮的体积比为:12:4=3:1,
故答案为:3:1.
点评:本题考查了有关混合物反应的计算,题目难度中等,根据氧化还原反应中化合价变化相等配平反应NOx+NH3→N2+H2O为解答关键,注意十字相乘法在化学计算中的应用方法.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
下列有关物质的组成、分类和化学用语正确的是( )
| A、油脂是由C、H、O三种元素组成的高分子化合物 |
| B、H2O、D2 O、T2 O互为同分异构体 |
C、CaC2的电子式为 |
| D、布朗运动是胶体的专有特性 |
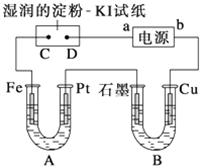 电解装置如图所示.图中B装置盛1L 2mol?L-1的Na2SO4溶液,A装置中盛1L 2mol?L-1AgNO3溶液.通电后,湿润的淀粉KI试纸的C端变蓝色.电解一段时间后,试回答:
电解装置如图所示.图中B装置盛1L 2mol?L-1的Na2SO4溶液,A装置中盛1L 2mol?L-1AgNO3溶液.通电后,湿润的淀粉KI试纸的C端变蓝色.电解一段时间后,试回答: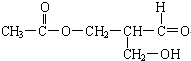 在有机物分子中碳原子所连的4个原子或原子团均不相同时,该碳原子叫手性碳原子,以*C表示.而且,该有机化合物具有光学活性.下列有机物是否具有光学活性?
在有机物分子中碳原子所连的4个原子或原子团均不相同时,该碳原子叫手性碳原子,以*C表示.而且,该有机化合物具有光学活性.下列有机物是否具有光学活性?