题目内容
下面是某些短周期元素的电负性:
(1)通过分析电负性变化规律,确定N、Mg的电负性取值范围: <x(N)< , <x(Mg)< .
(2)某有机化合物结构简式为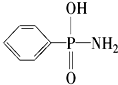 ,在P-N键中,你认为共用电子对偏向 (写原子名称).
,在P-N键中,你认为共用电子对偏向 (写原子名称).
| 元素符号 | 电负性 | 元素符号 | 电负性 |
| Li | 0.98 | Be | 1.57 |
| B | 2.04 | C | 2.55 |
| O | 3.44 | F | 3.98 |
| Na | 0.93 | Al | 1.61 |
| Si | 1.90 | P | 2.19 |
(2)某有机化合物结构简式为
 ,在P-N键中,你认为共用电子对偏向
,在P-N键中,你认为共用电子对偏向考点:元素电离能、电负性的含义及应用,不同晶体的结构微粒及微粒间作用力的区别
专题:元素周期律与元素周期表专题
分析:(1)同周期元素,从左到右电负性逐渐增大,同主族元素从下到上,电负性逐渐增大,电负性:C<N<O、P<N,Na<Mg<Al、Al<Be,结合表中数据作答;
(2)根据元素的电负性越强,原子吸电子能力越强,共用电子对就偏向于该元素.
(2)根据元素的电负性越强,原子吸电子能力越强,共用电子对就偏向于该元素.
解答:
解:(1)同周期元素,从左到右电负性逐渐增大,同主族元素从下到上,电负性逐渐增大,电负性:C<N<O、P<N,即为2.55<x(N)<3.44、2.19<x(N),
因此2.55<x(N)<3.44;
电负性:Na<Mg<Al、Al<Be,即为0.93<x(Mg)<1.61,x(Mg)<1.57,因此0.93<x(Mg)<1.57,
故答案为:2.55;3.44;0.93;1.57;
(2)根据元素的电负性越强,原子吸电子能力越强,共用电子对就偏向于该元素.电负性:N>P,所以共用电子对就偏向于N,故答案为:氮.
因此2.55<x(N)<3.44;
电负性:Na<Mg<Al、Al<Be,即为0.93<x(Mg)<1.61,x(Mg)<1.57,因此0.93<x(Mg)<1.57,
故答案为:2.55;3.44;0.93;1.57;
(2)根据元素的电负性越强,原子吸电子能力越强,共用电子对就偏向于该元素.电负性:N>P,所以共用电子对就偏向于N,故答案为:氮.
点评:本题考查电负性的递变规律,题目难度中等,注意元素周期律的主要内容,理解电负性的意义和应用.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
通常用来衡量一个国家石油化工发展水平标志的是( )
| A、乙烯的产量 |
| B、石油的产量 |
| C、原煤的产量 |
| D、硫酸的产量 |
下面有关晶体的叙述中,不正确的是( )
| A、金刚石为空间网状结构,由共价键形成的碳原子环上,最小的环上有6个碳原子 |
| B、氯化钠晶体中,每个Na+周围距离相等的Na+共有6个 |
| C、氯化铯晶体中,每个Cs+周围紧邻8个Cl- |
| D、干冰晶体中,每个CO2分子周围紧邻12个CO2分子 |
火箭升空时,由于与大气层的剧烈摩擦,产生高温.为了防止火箭表面温度过高,可在火箭表面涂上一种特殊的化学物质,该物质最可能具有的性质是( )
| A、硬度很大、熔点很高 |
| B、高温下可分解气化 |
| C、良好的热稳定性 |
| D、较强的还原性,易燃烧 |
已知Fe2+在水溶液中可以发生水解反应:Fe2++2H2O?Fe(OH)2+2H+.现欲配制硝酸亚铁溶液,为了防止Fe2+水解,可采取的措施为( )
| A、提高溶液碱性 | B、提高溶液酸性 |
| C、加水 | D、升温 |
不能用胶体的知识解释的现象是( )
| A、.向FeCl3溶液中加入NaOH溶液,出现红褐色沉淀 |
| B、石膏点豆腐 |
| C、.一支钢笔使用两种不同牌号的墨水,易出现堵塞 |
| D、.江河入海处,易形成沙洲 |