题目内容
2.下列说法正确的是( )| A. | Fe2(SO4)3溶液在空气中加热蒸干并灼烧后,可以得到Fe2(SO4)3 | |
| B. | 为除去MgCl2酸性溶液中的Fe3+,可在加热搅拌的条件下,加入氨水,过滤后向滤液中再加入适量盐酸 | |
| C. | 配制FeSO4溶液时,为了抑制亚铁离子水解,需加入少量Fe | |
| D. | 室温下,向PH=4的醋酸溶液中加入等体积的PH=10的NaOH溶液,反应后溶液呈碱性,是因为生成了强碱弱酸盐 |
分析 A.硫酸铁水解生成氢氧化铁和硫酸,当溶液蒸干时,得到的固体是硫酸铁;
B.除杂需要加入试剂调节溶液PH使铁离子沉淀,但不能引入新的杂质;
C.FeSO4溶液易被氧化为硫酸铁,加入铁可以防止Fe2+被氧化;
D.醋酸溶液中存在电离平衡,隋风云进行醋酸又电离出氢离子.
解答 解:A.硫酸铁水解生成氢氧化铁和硫酸,加热促进硫酸铁水解,因为硫酸没有挥发性,所以得到的固体仍然是Fe2(SO4)3,硫酸铁水解离子方程式为Fe3++3H2O?Fe(OH)3+3H+,故A正确;
B.加入氨水混入氯化铵杂质,且生成氢氧化镁沉淀,故B错误;
C.FeSO4溶液易被氧化为硫酸铁,加入铁可以防止Fe2+被氧化,不是抑制水解,故C错误;
D.室温下,向PH=4的醋酸溶液中加入等体积的PH=10的NaOH溶液,反应后促进醋酸电离,溶液呈酸性,故D错误;
故选A.
点评 本题考查了盐类水解、除杂方法、酸碱反应后溶液酸碱性判断,注意弱电解质电离平衡的分析,掌握基础是解题关键,题目难度中等.

练习册系列答案
相关题目
12.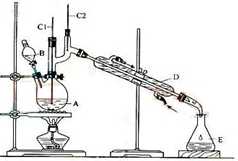 正丁醛是一种化工原料.某实验小组利用如图装置合成正丁醛.
正丁醛是一种化工原料.某实验小组利用如图装置合成正丁醛.
Na2Cr2O7H2SO4加热
发生的反应如下:
CH3CH2CH2CH2OH$\frac{\underline{\;\;\;Na_{2}Cr_{2}O_{7}\;\;\;}}{H_{2}SO_{4}加热}$ CH3CH2CH2CHO
反应物和产物的相关数据列表如表:
实验步骤如下:
将6.0gNa2Cr2O7放入100mL烧杯中,加30mL水溶解,再缓慢加入5mL浓硫酸,将所得溶液小心转移至B中.在A中加入4.0g正丁醇和几粒沸石,加热.当有蒸汽出现时,开始滴加B中溶液.滴加过程中保持反应温度为90-95℃,在E中收集90℃以下的馏分.将馏出物倒入分液漏斗中,分去水层,有机层干燥后蒸馏,收集75-77℃馏分,产量2.4g.回答下列问题:
(1)实验中,能否将Na2Cr2O7溶液加到浓硫酸中,说明理由不能,浓硫酸溶于水会放出大量热,容易溅出伤人.
(2)加入沸石的作用是防止液体暴沸.若加热后发现未加沸石,应采取的正确方法是冷却后补加.
(3)装置图中,D仪器的名称是滴液漏斗,B仪器的名称是直形冷凝管,冷水从下进.(填上或下)
(4)分液漏斗使用前必须进行的操作是b(填正确答案标号).
a.润湿 b.检漏 c.干燥 d.标定
(5)将正丁醛粗产品置于分液漏斗中分层时,水在下 层(填“上”或“下”)
(6)本实验中,正丁醛的产率为62.5%.
(7)反应温度应保持在90-95℃,其原因是保证正丁醛及时蒸出,又可尽量避免其被进一步氧化.
 正丁醛是一种化工原料.某实验小组利用如图装置合成正丁醛.
正丁醛是一种化工原料.某实验小组利用如图装置合成正丁醛.Na2Cr2O7H2SO4加热
发生的反应如下:
CH3CH2CH2CH2OH$\frac{\underline{\;\;\;Na_{2}Cr_{2}O_{7}\;\;\;}}{H_{2}SO_{4}加热}$ CH3CH2CH2CHO
反应物和产物的相关数据列表如表:
| 沸点/℃ | 密度/(g•cm-3) | 水中溶解性 | |
| 正丁醇 | 117.72 | 0.8109 | 微溶 |
| 正丁醛 | 75.7 | 0.8017 | 微溶 |
将6.0gNa2Cr2O7放入100mL烧杯中,加30mL水溶解,再缓慢加入5mL浓硫酸,将所得溶液小心转移至B中.在A中加入4.0g正丁醇和几粒沸石,加热.当有蒸汽出现时,开始滴加B中溶液.滴加过程中保持反应温度为90-95℃,在E中收集90℃以下的馏分.将馏出物倒入分液漏斗中,分去水层,有机层干燥后蒸馏,收集75-77℃馏分,产量2.4g.回答下列问题:
(1)实验中,能否将Na2Cr2O7溶液加到浓硫酸中,说明理由不能,浓硫酸溶于水会放出大量热,容易溅出伤人.
(2)加入沸石的作用是防止液体暴沸.若加热后发现未加沸石,应采取的正确方法是冷却后补加.
(3)装置图中,D仪器的名称是滴液漏斗,B仪器的名称是直形冷凝管,冷水从下进.(填上或下)
(4)分液漏斗使用前必须进行的操作是b(填正确答案标号).
a.润湿 b.检漏 c.干燥 d.标定
(5)将正丁醛粗产品置于分液漏斗中分层时,水在下 层(填“上”或“下”)
(6)本实验中,正丁醛的产率为62.5%.
(7)反应温度应保持在90-95℃,其原因是保证正丁醛及时蒸出,又可尽量避免其被进一步氧化.
10.下列物质中,不能发生水解反应的是( )
| A. | 纤维素 | B. | 淀粉 | C. | 葡萄糖 | D. | 蛋白质 |
17.一定温度下的密闭容器中,反应 2SO2(g)+O2(g)?2SO3 (g) 达到平衡.缩小容器容积,对反应产生影响的叙述不正确的是( )
| A. | 使 SO3 的浓度增大 | B. | 使平衡向正反应方向移动 | ||
| C. | 使平衡常数 K 增大 | D. | 使正反应速率大于逆反应速率 |
7.向一容积为5L的恒容密闭容器中充入5molA与8molB,在一定条件下反应:2A(g)+3B(g)?xC(g)+yD(g) (x、y为正整数),反应进行2min后达到平衡,这2min内平均反应速率v(C)=0.3mol/(L•min),D的平衡浓度为0.3mol/L,又知v(B):v(C)=3:2,则下列说法中正确的是( )
| A. | x:y=3:1 | B. | v(A):v(C)=2:1 | ||
| C. | A的平衡浓度为0.4mol/L | D. | A与B的平衡浓度之比为3:2 |
14.用NA表示阿伏加德罗常数,下列有关说法正确的是( )
| A. | 标准状况下,22.4 L 水蒸气含有的分子数为1NA | |
| B. | 常温常压下,32 g O2含有的原子数为2个 | |
| C. | 常温常压下,NA个CO2分子占有的体积为22.4 L | |
| D. | 体积为1L、物质的量浓度为0.5 mol/L的氯化钙溶液中,含有Cl-个数为1NA |
11.下列变化中,一定不存在化学能与热能相互转化的是( )
| A. | 铝热反应 | B. | 干冰气化 | C. | 燃放爆竹 | D. | Zn粉与盐酸反应 |