题目内容
11.设nA为阿伏加德罗常数的数值,下列说法正确的是( )| A. | 常温常压下,8gO2含有4nA个电子 | |
| B. | 标准状况下22.4 L的NH3溶于水,所得溶液中有nA个NH4+ | |
| C. | 200mL的5mol•L-1盐酸中含有nA个HCl分子 | |
| D. | 1mol Na被完全氧化生成Na2O2,失去2nA个电子 |
分析 A、求出氧气的物质的量,然后根据1mol氧气中含16mol电子来分析;
B、氨气溶于水生成的一水合氨是弱电解质,不能完全电离;
C、盐酸溶液中无HCl分子;
D、根据反应后钠元素变为+1价来分析.
解答 解:A、8g氧气的物质的量为0.25mol,而1mol氧气中含16mol电子,故0.25mol氧气中含4mol电子即4nA个,故A正确;
B、氨气溶于水生成的一水合氨是弱电解质,不能完全电离,故所得溶液中的铵根离子的个数小于nA个,故B错误;
C、HCl溶于水后完全电离为氢离子和氯离子,故盐酸溶液中无HCl分子,故C错误;
D、由于反应后钠元素变为+1价,故1mol钠失去1mol电子即nA个,故D错误.
故选A.
点评 本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,难度不大.

练习册系列答案
相关题目
1.下列叙述中正确的是( )
| A. | 电离时能够产生H+的化合物是酸 | |
| B. | 难溶的物质(如CaCO3)不能发生离子反应 | |
| C. | 电解质在水中不一定能导电,在水中导电的化合物不一定是电解质 | |
| D. | 胶体加入电解质可产生沉淀,而溶液不能 |
2.用1L的1.0mol•L-1NaOH 溶液吸收0.7molCO2,所得溶液中的CO32-和HCO3-的浓度之比约是 ( )
| A. | 1:2 | B. | 1:3 | C. | 2:3 | D. | 3:4 |
19.下列有关物质用途的叙述中,错误的是( )
| A. | 液氨常被用作制冷剂 | |
| B. | 可利用2Fe3++Cu═Cu2++2Fe2+腐蚀印刷电路板 | |
| C. | 为便于储存和使用,可用液氯代替氯水漂白干燥棉布上的有色物质为便于储存和使用,可用液氯代替氯水漂白干燥棉布上的有色物质 | |
| D. | 已知3Cl2+2NH3═N2+6HCl,工业上可用浓氨水检查氯气管道是否漏气 |
6.下列说法不正确的是( )
| A. | 探究温度对反应速率影响时,分别水浴加热硫代硫酸钠溶液、硫酸溶液到一定温度,再将两溶液混合 | |
| B. | 用简易量热计测定反应热,使用碎泡沫隔热保温、环形玻璃搅拌棒搅拌、量取达到的最高温度,计算反应热,取2~3 次的实验平均值 | |
| C. | H2O2在过氧化氢酶的催化下,随着温度的升高,分解速率持续加快 | |
| D. | 欲粗略测定某未知浓度的醋酸溶液中醋酸的电离常数Ka,应做的实验和所需的试剂(或试纸)分别为中和滴定实验和pH试纸 |
16.将一定量纯净的氨基甲酸铵置于密闭真空恒容容器中(固体试样体积忽略不计),在恒定温度下使其达到分解平衡:NH2COONH4(s)?2NH3(g)+CO2(g).判断该分解反应已经达到化学平衡的是( )
| A. | 2v(NH3)=v(CO2) | B. | 密闭容器中c(NH3):c(CO2)=2:1 | ||
| C. | 密闭容器中体积不变 | D. | 密闭容器中混合气体的密度不变 |
3.下列溶液中,能用来区别SO2和CO2气体的是( )
①石灰水 ②H2S溶液 ③KMnO4溶液 ④紫色石蕊溶液 ⑤BaCl2溶液 ⑥品红溶液.
①石灰水 ②H2S溶液 ③KMnO4溶液 ④紫色石蕊溶液 ⑤BaCl2溶液 ⑥品红溶液.
| A. | ①④⑤ | B. | ②④⑤ | C. | ③④⑤ | D. | ②③⑥ |
20.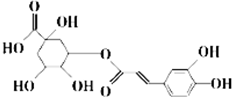 中成药银翘中含有具有较广泛抗菌作用的有效成分--绿原酸,其结构简式如图所示.下列有关说法不正确的是( )
中成药银翘中含有具有较广泛抗菌作用的有效成分--绿原酸,其结构简式如图所示.下列有关说法不正确的是( )
 中成药银翘中含有具有较广泛抗菌作用的有效成分--绿原酸,其结构简式如图所示.下列有关说法不正确的是( )
中成药银翘中含有具有较广泛抗菌作用的有效成分--绿原酸,其结构简式如图所示.下列有关说法不正确的是( )| A. | 绿原酸可通过酯化反应人工合成 | |
| B. | 1 mol绿原酸能与2molBr2发生加成反应 | |
| C. | 1mol绿原酸能与6molNa发生置换反应 | |
| D. | 绿原酸能与NaHCO3溶液发生复分解反应 |