题目内容
【题目】(1)某温度下,H2O的离子积常数为1×10-13,则该温度下0.01mol/L NaOH溶液的pH=________
(2) 25℃时,将amol/L的氨水与0.01mol/L的盐酸等体积混合,反应后溶液中c (NH4+) =c (Cl-),则溶液呈______(填“酸”、“碱”或“中”)性,用含a的代数式表示NH3·H2O 的电离平衡常数 Kb=____
【答案】 11 中 ![]()
【解析】(1)溶液中c(H+)=![]() mol/L=10-11mol/L,pH=-lgc(H+)=-lg10-11=11,故答案为:11;
mol/L=10-11mol/L,pH=-lgc(H+)=-lg10-11=11,故答案为:11;
(2)在25℃下,平衡时溶液中c(NH4+)=c(Cl-)=0.005mol/L,根据物料守恒得c(NH3H2O)=(0.5a-0.005)mol/L,根据电荷守恒得c(H+)=c(OH-)=10-7mol/L,溶液呈中性,NH3H2O的电离常数Kb=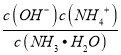 =
=![]() =
=![]() ,故答案为:中;
,故答案为:中; ![]() 。
。

练习册系列答案
 教材全解字词句篇系列答案
教材全解字词句篇系列答案
相关题目
