题目内容
16.用NA表示阿伏加德罗常数,N表示粒子数,下列说法正确的是( )| A. | 7.8 g苯含有碳碳双键的数目为0.3NA | |
| B. | 标准状况下,足量的Fe与2.24 L Cl2反应转移电子的数目为0.3NA | |
| C. | 1.6 g CH4含有共用电子对的数目为0.5NA | |
| D. | 100mLpH=2的新制氯水中,:N(OH-)+2N(ClO-)+N(HClO)=0.001NA |
分析 A、苯不是单双键交替的结构;
B、由于铁是过量的,故转移电子数根据氯气的量来计算;
C、求出甲烷的物质的量,然后根据1mol甲烷中含4mol共用电子对来分析;
D、根据电荷守恒:N(H+)=N(OH-)+N(ClO-)+N(Cl-)分析.
解答 解:A、苯不是单双键交替的结构,故苯中不含碳碳双键,故A错误;
B、由于铁是过量的,故转移电子数根据氯气的量来计算.标况下,2.24氯气的物质的量为0.1mol,反应后氯元素变为-1价,故0.1mol氯气转移0.2mol电子,即0.2NA个,故B错误;
C、1.6g烷的物质的量为0.1mol,而1mol甲烷中含4mol共用电子对,故0.1mol甲烷含0.4mol共用电子对,故C错误;
D、100mL pH=2的新制氯水中,溶液中的电荷守恒:N(H+)=N(OH-)+N(ClO-)+N(Cl-),N(H+)=0.001NA,则N(OH-)+N(ClO-)+N(Cl-)=0.001NA,氯气与水反应生成次氯酸,生成的盐酸与次氯酸电离出的氯离子与次氯酸根离子相等,根据物料守恒,N(Cl-)=N(ClO-)+N(HClO),联合物料守恒和电荷守恒可得出N(OH-)+2N(ClO-)+N(HClO)=0.001NA,故D正确.
故选D.
点评 本题考查了阿伏伽德罗常数的有关运用,难度不到,熟练掌握公式的运用和物质的性质是解题关键.

练习册系列答案
相关题目
6.下列用电子式表示化合物的形成过程,正确的是( )
| A. |  | |
| B. | 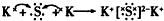 | |
| C. | 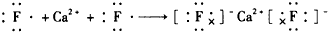 | |
| D. |  |
7.绿色农药信息素的推广使用,对环保有重要意义.有一种信息素的结构简式为CH3(CH2)5CH=CH(CH2)9CHO.下列关于检验该信息素中官能团的试剂和顺序正确的是( )
| A. | 先加入酸性高锰酸钾溶液;加稀硝酸酸化后加银氨溶液,微热 | |
| B. | 先加入溴水;加稀硝酸酸化后加酸性高锰酸钾溶液 | |
| C. | 先加入新制氢氧化铜悬浊液,加热;加稀硝酸酸化,再加入溴水 | |
| D. | 先加入银氨溶液;再另取该物质加入溴水 |
4.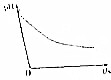 某离子反应涉及H2O、CLO-、NH4+、H+、N2、CL-六种微粒.常温条件下反应时,溶液pH随时间变化的曲线如图所示,下列判断错误的是( )
某离子反应涉及H2O、CLO-、NH4+、H+、N2、CL-六种微粒.常温条件下反应时,溶液pH随时间变化的曲线如图所示,下列判断错误的是( )
 某离子反应涉及H2O、CLO-、NH4+、H+、N2、CL-六种微粒.常温条件下反应时,溶液pH随时间变化的曲线如图所示,下列判断错误的是( )
某离子反应涉及H2O、CLO-、NH4+、H+、N2、CL-六种微粒.常温条件下反应时,溶液pH随时间变化的曲线如图所示,下列判断错误的是( )| A. | 该反应的氧化剂是CLO- | |
| B. | 该反应中有两种离子生成 | |
| C. | 该反应生成1mol氧化产物时,转移的电子为6mol | |
| D. | 参加反应的氧化剂与还原剂的物质的量之比为2:3 |
8.W、X、Y、Z为短周期主族元素,原子序数依次增加,W的一种核素在考古时常用来鉴定一些文物的年代.化合物XZ是重要的调味品,Y原子的最外层电子数等于其电子层数,Z-的电子层结构与氩相同.下列说法错误的是( )
| A. | 元素W与氢形成原子比为1:1的化合物有多种 | |
| B. | 元素X的单质能与水、无水乙醇反应 | |
| C. | 离子Y3+与Z-的最外层电子数和电子层数都不相同 | |
| D. | 元素W与元素Z可形成含有极性共价键的化合物 |
17.用NA表示阿伏加德罗常数的值,下列说法正确的是( )
| A. | 56g Fe与稀HNO3完全反应时一定转移3NA个电子 | |
| B. | 标准状况下11.2 L NH3溶于1 L水中,溶液中含N原子的微粒总数为0.5NA | |
| C. | 常温常压下,0.1NA个Al与足量氢氧化钠溶液反应生成3.36 LH2 | |
| D. | 同温同压下,H2(g)+Cl2(g)=2HCl(g)在光照和点燃条件下的△H不同 |